技术摘要:
本发明属于有机导体技术领域,具体涉及一类N‑型中性双自由基导电化合物及其制备方法和应用。本发明制备的式(I)化合物具有刚性大π‑共轭平面和强的双自由基特性,具有优异的导电性能。而且,本发明制备的式(I)化合物具有易于官能化的特点,可以借助杂环的芳香性实现自 全部
背景技术:
导电是有机共轭材料的重要特性之一,在有机自旋器件,超导体,热电器件等领域 有着广阔的前景(R.C.Haddon .Nature .1975 ,256 ,394 .X .Chi ,M .E.Itkis ,B.O .Patrick , T.M.Barclay,R.W.Reed,R.T.Oakley,A.W.Cordes,R.C.Haddon,J.Am.Chem.Soc.1999,121, 10395.)。近年来,中性单组份有机导体尤其受到广泛的关注,这主要是由于其制备简单,性 能可控(Y .Kobayashi ,T .Terauchi ,S .Sumi ,Y .Matsushita ,Nat .Mater .2017 ,16 , 109 .Y .Joo ,V .Agarkar ,S .H .Sung ,B .M .Savoie ,B .W .Boudouris ,Science .2018 ,359 , 1391.A.Mailman,A.A.Leitch,W.Yong ,E.Steven,S.M.Winter,R.C.Claridge,A.Assoud , J.S.Tse,S.Desgreniers,R.A.Secco,R.T.Oakley,J.Am.Chem.Soc.2017,139,2180.)。此 外,基于中性单组份有机化合物导体在信息读写、生物传感和超导等方面也有着重要应用 前景(Itkis,M.E.;Chi,X.;Cordes,A.W.;Haddon,R.C.Science.2002,296,1443.Pal,S.K.; Itkis ,M .E .;Tham ,F .S .;Reed ,R .W .;Oakley ,R .T .;Haddon ,R .C .Science .2005 ,309 , 281.Joo,Y.;Huang ,L.;Eedugurala ,N.;London,A.E.;Kumar,A.;Wong ,B.M.;Boudouris, B.W.;Azoulay,J.D.Macromolecules.2018,51,3886.)。相对于大量基于电荷转移复合物的 有机导体,单组份有机导体材料受窄能带宽度和宽导带-价带带隙的能级限制,种类较少, 主要为TTF (U e d a ,K .;Ka m a ta ,Y .;Iwa m a t s u ,M .;Sug i m o t o ,T .;F u j i ta , H .J .Mater .Chem .1999 ,9 ,2979 .Tanaka ,H .;Okano ,Y .;Kobayashi ,H .;Suzuki ,W .; Kobayashi,A.Science.2001,291,285.Kobayashi,Y.;Yoshioka,M.;Saigo,K.;Hashizume, D.;Ogura,T.J.Am.Chem.Soc.2009,131 9995.Isono,T.;Kamo,H.;Ueda,A.;Takahashi,K.; Nakao,A.;Kumai,R.;Nakao,H.;Kobayashi,K.;Murakami,Y.;Mori,H.Nat.Commun.2013,4, 1344 .))和PLY(Chi ,X .;Itkis ,M .E .;Kirschbaum ,K .;Pinkerton ,A .A .;Oakley ,R .T .; Cordes ,A .W .Pal ,S .K .;Itkis ,M .E .;Tham ,F .S .;Reed ,R .W .;Oakley ,R .T .;Haddon , R .C .Science .2005 ,309 ,281 .C .J .Am .Chem .Soc .2001 ,123 ,4041 .Bag ,P.;Itkis ,M .E .; Stekovic,D.;Pal,S.K.;Tham,F.S.;Haddon,R.C.J.Am.Chem.Soc.2015,137,10000.)衍生 物。一般而言,绝大部分中性单组份有机导体都是单自由基导体并且没有N-型导体报道,醌 式双自由基几乎没有被考虑为导体。
技术实现要素:
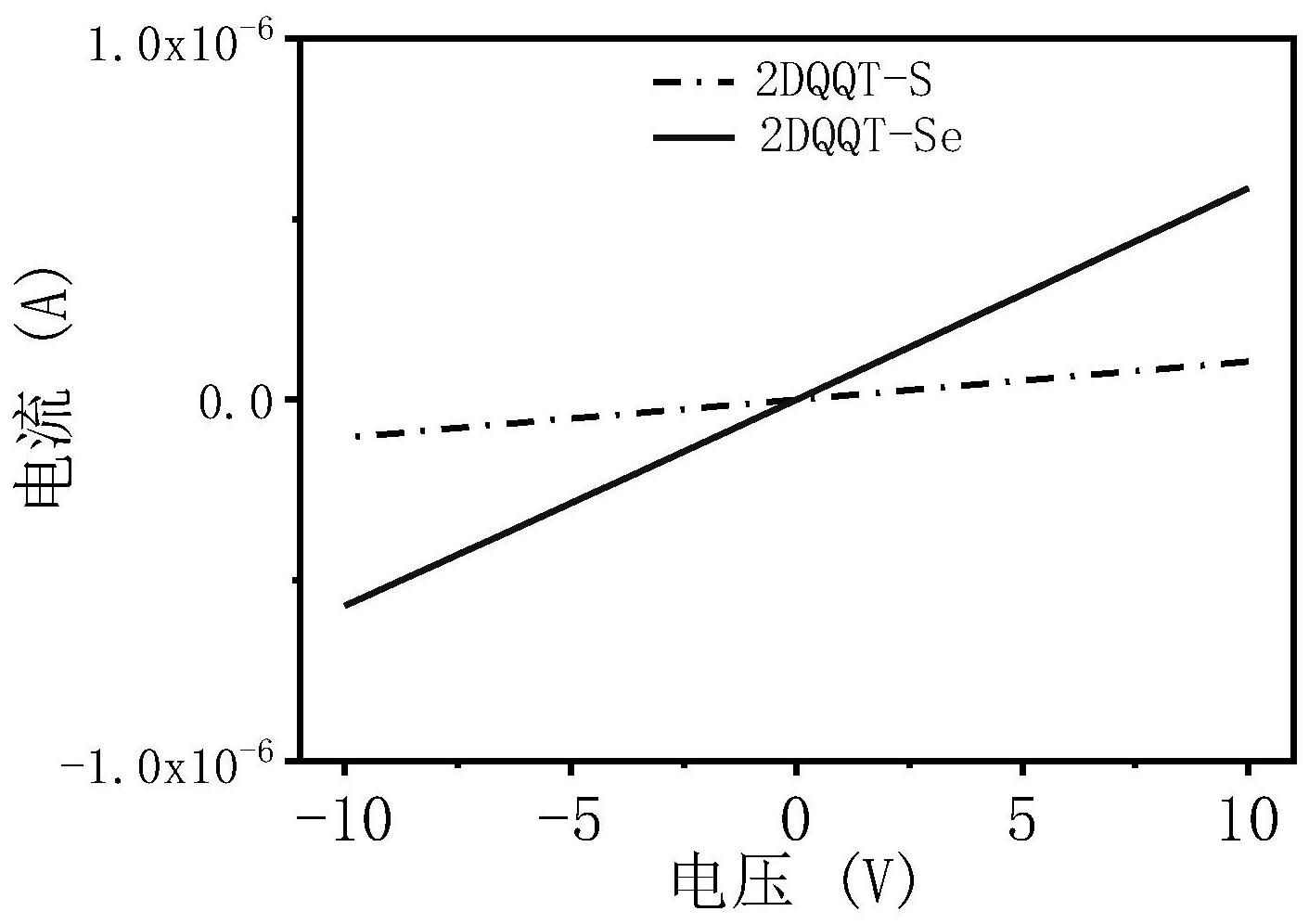
为改善上述技术问题,本发明提供下式(I)所示化合物: 7 CN 111548359 A 说 明 书 2/10 页 其中,每一个R1相同或不同,彼此独立地选自:氢、卤素、氰基、无取代或任选被一 个、两个或更多个Ra取代的下列基团:C1-40烷基、C1-40烷氧基、C3-20环烷基、C3-20环烷基氧基、 3-20元杂环基、3-20元杂环基氧基、C6-20芳基、C6-20芳基氧基、5-20元杂芳基、5-20元杂芳基 氧基、-(O-(CH2)n-O)mH、-COO-R3、-CO-R4; 每一个R2相同或不同,彼此独立地选自:氢、卤素、氰基、无取代或任选被一个、两 个或更多个Rb取代的下列基团:C1-40烷基、C1-40烷氧基、C3-20环烷基、C3-20环烷基氧基、3-20元 杂环基、3-20元杂环基氧基、C6-20芳基、C6-20芳基氧基、5-20元杂芳基、5-20元杂芳基氧基、- (O-(CH2)n-O)mH、-COO-R3、-CO-R4; 其中,m、n相同或不同,彼此独立地选自1-8的整数,优选1-6的整数; 所述R3、R4相同或不同,彼此独立地选自H、C1-40烷基、C3-20环烷基、3-20元杂环基、 C6-20芳基、5-20元杂芳基; 每一个R5、R7、R8相同或不同,彼此独立地选自:O(氧)、S(硫)、Se(硒)、Te(碲)、CR9; 所述R9选自H、无取代或任选被一个、两个或更多个Rc取代的下列基团:C1-40烷基、C2-40烯基、 C2-40炔基、C1-40烷氧基、C3-20环烷基、3-20元杂环基、C6-20芳基、C6-20芳基氧基、5-20元杂芳基、 5-20元杂芳基氧基; 每一个R6相同或不同,彼此独立地选自:CH、N; 每一个Ra、Rb、Rc相同或不同,彼此独立地选自-F、-Cl、-Br、-I、-OH、-SH、-CN、=O、- NO2、-NH2、卤代C1-40烷基、卤代C1-40烷基氧基、C1-40烷基、C1-40烷氧基、C1-40烷基硫基、C2-40烯 基、C2-40烯基氧基、C2-40烯基硫基、C2-40炔基、C2-40炔基氧基、C2-40炔基硫基、C3-20环烷基、C3-20 环烷基氧基、C3-20环烷基硫基、3-20元杂环基、3-20元杂环基氧基、3-20元杂环基硫基、C6-20 芳基、C6-20芳基氧基、C6-20芳基硫基、5-20元杂芳基、5-20元杂芳基氧基、5-20元杂芳基硫基。 在一个优选实施方式中,所述式(I)化合物具有如下结构: 8 CN 111548359 A 说 明 书 3/10 页 其中,R1、R2、R5、R6、R7、R8具有上述定义; 在一个优选实施方式中,每一个R1相同或不同,彼此独立地选自:氢、卤素、无取代 或任选被一个、两个或更多个Ra取代的下列基团:C1-40烷基、C1-40烷氧基、-(O-(CH2)n-O)mH、 C6-20芳基;所述m、n相同或不同,彼此独立地选自1-3的整数;优选地,Ra可以选自-F、-Cl、- Br、-I;优选地,所述R1可以选自氢、氟、氯、三氟甲基、苯基、正己基; 在一个优选实施方式中,每一个R2相同或不同,彼此独立地选自:氰基、无取代或 任选被一个、两个或更多个Rb取代的下列基团:C1-40烷基、C1-40烷氧基、-(O-(CH2)n-O)mH、- COO-R3、-CO-R4、C6-20芳基;所述m、n相同或不同,彼此独立地选自1-3的整数;所述Rb、R3、R4具 有上文所述定义;例如,R2可以选自 每一个R5、R7、R8相同或不同,彼此独立地选自:O、S、Se、Te、CR9;所述R9例如选自H; 每一个R6相同或不同,彼此独立地选自:CH、N。 作为实例,所述式(I)化合物选自如下具体化合物: 9 CN 111548359 A 说 明 书 4/10 页 本发明还提供上述式(I)化合物的制备方法,包括以下步骤: A)式(II)化合物与丙二腈、氧化剂进行反应,得到式(I)化合物; 其中,R”’为卤素(例如氟、氯、溴、碘),R1、R2、R5、R6、R7、R8具有上述定义。 根据本发明, 所述制备方法具体为:式(II)化合物与丙二腈进行反应;随后加入氧化剂进行反 应,得到式(I)化合物; 所述反应可以在溶剂中进行,所述溶剂选自醚类溶剂,例如1,4-二氧六环; 进一步地,式(II)化合物与丙二腈进行反应时,所述反应可以加入碱、催化剂;所 述反应可以在加热条件下进行,优选在加热回流下进行;所述反应的时间可以为2-6小时, 10 CN 111548359 A 说 明 书 5/10 页 例如4小时; 所述碱优选为强碱;所述强碱例如选自氢化钠; 所述催化剂选自钯催化剂,例如四三苯基膦钯; 进一步地,式(II)化合物与丙二腈反应结束后;优选将反应体系冷却,例如冷却至 室温;随后向反应体系中加入氧化剂,进行反应;所述反应可以加入酸,所述酸可以选自盐 酸,例如盐酸溶液;所述反应的时间可以为0.5-2小时,例如1小时; 所述氧化剂可以选自2,3-二氯-5,6二氰苯醌; 根据本发明,所述制备方法具体为:先将强碱和丙二腈溶于溶剂中,搅拌后,再加 入式(II)化合物和催化剂,加热回流。冷却至室温后,加入盐酸和氧化剂。 根据本发明,所述式(II)化合物可以通过如下方法制备,包括: 1)式(IV)化合物与式(V)化合物混合,得到式(III)化合物; 2)式(III)化合物与卤化剂进行反应,生成式(II)化合物; 其中,R’为有机锡基,例如三正丁基锡基、三甲基锡基;R”、R”’相同或不同,彼此独 立地选自氟、氯、溴、碘;R1、R2、R5、R6、R7、R8具有上述定义。 根据本发明,步骤1)中, 所述反应可以加入催化剂,所述催化剂选自钯催化剂,例如四三苯基膦钯。 所述反应可以在溶剂中进行,所述溶剂选自芳烃类溶剂、酰胺类溶剂中的至少一 种,例如选自甲苯和N,N-二甲基甲酰胺(DMF)的混合溶剂,两者的体积比可以为1:1; 所述反应的温度可以为50-130℃,例如90℃。 所述反应的时间可以为12-36小时,例如48小时。 根据本发明,步骤2)中, 所述卤化剂包括氟化剂、氯化剂、溴化剂、碘化剂;例如,所述溴化剂选自N-溴代丁 二酰亚胺。 所述反应可以在溶剂中进行,所述溶剂选自卤代烃类溶剂、酰胺类溶剂中的至少 一种,例如三氯甲烷和N,N-二甲基甲酰胺的混合溶剂,两者的体积比可以为3:1。 所述反应可以在室温下进行。 所述反应的时间可以为1-3小时,例如2小时。 根据本发明,所述式(II)化合物的制备方法可以具体为:先将式(IV)化合物、式 (V)化合物溶于溶剂中,加入四三苯基膦钯,于90℃避光搅拌两天。将所得式(III)化合物溶 于溶剂,避光加入NBS,室温搅拌两小时。 本发明还提供所述式(I)化合物的用途,其可作为热电材料,用于可穿戴供电设备 11 CN 111548359 A 说 明 书 6/10 页 或微型制冷设备中。 本发明的有益效果在于: 1 .本发明制备的式(I)化合物具有刚性大π-共轭平面和强的双自由基特性,具有 优异的导电性能。本发明的式(I)化合物是平面型分子,其结构固定,没有异构体。所述化合 物电导率高,而且具有电子型主导的载流子导电的特有性质。通过理论计算和能谱分析得 知其高电导的特有性质与其特有的强双自由基特性有关。 本发明的式(I)化合物具有刚性平面分子结构,狭窄的导带-价带带隙,导致闭壳 醌式向开壳芳香双自由基转化所需的活化能小,从而实现缺电子醌式结构和富电子的芳香 结构共存,并发生自掺杂,诱导载流子的生成。所以该类双自由基分子的导电很强。本发明 的式(I)化合物涵盖了不同的双自由基强度,通过噻吩和硒吩的不同芳香性可以调控化合 物的双自由基强度,其最强双自由基特征值为0.52(量子化学计算:(U)CAM-B3LYP/6-31G (d,p))。通过四探针法测试其薄膜水平方向的电导率高达0.29S cm-1。醌式四噻吩共轭分子 高度空气稳定性和高电导率适用于N-型有机热电材料和电子传输层的应用。其中热电性能 的功率因子高达1.4μW m-1K-2。 2.本发明制备的式(I)化合物具有易于官能化的特点,可以借助杂环的芳香性实 现自掺杂程度的有效调控。 3.本发明式(I)化合物的制备方法简单,产品收率高,适于工业化的大规模生产。 术语定义和说明 除非另有说明,本申请说明书和权利要求书中记载的基团和术语定义,包括其作 为实例的定义、示例性的定义、优选的定义、表格中记载的定义、实施例中具体化合物的定 义等,可以彼此之间任意组合和结合。这样的组合和结合后的基团定义及化合物结构,应当 属于本申请说明书记载的范围内。 术语“卤素”应理解为氟、氯、溴、碘。 术语“C1-40烷基”应理解为优选表示具有1~40个碳原子的直链或支链饱和一价烃 基,优选为C1-10烷基。“C1-10烷基”应理解为优选表示具有1、2、3、4、5、6、7、8、9或10个碳原子 的直链或支链饱和一价烃基。所述烷基是例如甲基、乙基、丙基、丁基、戊基、己基、异丙基、 异丁基、仲丁基、叔丁基、异戊基、2-甲基丁基、1-甲基丁基、1-乙基丙基、1,2-二甲基丙基、 新戊基、1,1-二甲基丙基、4-甲基戊基、3-甲基戊基、2-甲基戊基、1-甲基戊基、2-乙基丁基、 1-乙基丁基、3,3-二甲基丁基、2,2-二甲基丁基、1,1-二甲基丁基、2,3-二甲基丁基、1,3-二 甲基丁基或1,2-二甲基丁基等或它们的异构体。特别地,所述基团具有1、2、3、4、5、6个碳原 子(“C1-6烷基”),例如甲基、乙基、丙基、丁基、异丙基、异丁基、仲丁基、叔丁基,更特别地,所 述基团具有1、2或3个碳原子(“C1-3烷基”),例如甲基、乙基、正丙基或异丙基。 术语“C2-40烯基”应理解为优选表示直链或支链的一价烃基,其包含一个或多个双 键并且具有2~40个碳原子,优选“C2-10烯基”。“C2-10烯基”应理解为优选表示直链或支链的 一价烃基,其包含一个或多个双键并且具有2、3、4、5、6、7、8、9或10个碳原子,特别是2或3个 碳原子(“C2-3烯基”),应理解,在所述烯基包含多于一个双键的情况下,所述双键可相互分 离或者共轭。所述烯基是例如乙烯基、烯丙基、(E)-2-甲基乙烯基、(Z)-2-甲基乙烯基、(E)- 丁-2-烯基、(Z)-丁-2-烯基、(E)-丁-1-烯基、(Z)-丁-1-烯基、戊-4-烯基、(E)-戊-3-烯基、 (Z)-戊-3-烯基、(E)-戊-2-烯基、(Z)-戊-2-烯基、(E)-戊-1-烯基、(Z)-戊-1-烯基、己-5-烯 12 CN 111548359 A 说 明 书 7/10 页 基、(E)-己-4-烯基、(Z)-己-4-烯基、(E)-己-3-烯基、(Z)-己-3-烯基、(E)-己-2-烯基、(Z)- 己-2-烯基、(E)-己-1-烯基、(Z)-己-1-烯基、异丙烯基、2-甲基丙-2-烯基、1-甲基丙-2-烯 基、2-甲基丙-1-烯基、(E)-1-甲基丙-1-烯基、(Z)-1-甲基丙-1-烯基、3-甲基丁-3-烯基、2- 甲基丁-3-烯基、1-甲基丁-3-烯基、3-甲基丁-2-烯基、(E)-2-甲基丁-2-烯基、(Z)-2-甲基 丁-2-烯基、(E)-1-甲基丁-2-烯基、(Z)-1-甲基丁-2-烯基、(E)-3-甲基丁-1-烯基、(Z)-3- 甲基丁-1-烯基、(E)-2-甲基丁-1-烯基、(Z)-2-甲基丁-1-烯基、(E)-1-甲基丁-1-烯基、 (Z)-1-甲基丁-1-烯基、1,1-二甲基丙-2-烯基、1-乙基丙-1-烯基、1-丙基乙烯基、1-异丙基 乙烯基。 术语“C2-40炔基”应理解为表示直链或支链的一价烃基,其包含一个或多个三键并 且具有2~40个碳原子,优选“C2-C10炔基”。术语“C2-C10炔基”应理解为优选表示直链或支链 的一价烃基,其包含一个或多个三键并且具有2、3、4、5、6、7、8、9或10个碳原子。所述炔基是 例如乙炔基、丙-1-炔基、丙-2-炔基、丁-1-炔基、丁-2-炔基、丁-3-炔基、戊-1-炔基、戊-2- 炔基、戊-3-炔基、戊-4-炔基、己-1-炔基、己-2-炔基、己-3-炔基、己-4-炔基、己-5-炔基、1- 甲基丙-2-炔基、2-甲基丁-3-炔基、1-甲基丁-3-炔基、1-甲基丁-2-炔基、3-甲基丁-1-炔 基、1-乙基丙-2-炔基、3-甲基戊-4-炔基、2-甲基戊-4-炔基、1-甲基戊-4-炔基、2-甲基戊- 3-炔基、1-甲基戊-3-炔基、4-甲基戊-2-炔基、1-甲基戊-2-炔基、4-甲基戊-1-炔基、3-甲基 戊-1-炔基、2-乙基丁-3-炔基、1-乙基丁-3-炔基、1-乙基丁-2-炔基、1-丙基丙-2-炔基、1- 异丙基丙-2-炔基、2,2-二甲基丁-3-炔基、1,1-二甲基丁-3-炔基、1,1-二甲基丁-2-炔基或 3,3-二甲基丁-1-炔基。特别地,所述炔基是乙炔基、丙-1-炔基或丙-2-炔基。 术语“C3-20环烷基”应理解为表示饱和的一价单环或双环烃环,其具有3~20个碳 原子,优选“C3-10环烷基”。术语“C3-10环烷基”应理解为表示饱和的一价单环或双环烃环,其 具有3、4、5、6、7、8、9或10个碳原子。所述C3-10环烷基可以是单环烃基,如环丙基、环丁基、环 戊基、环己基、环庚基、环辛基、环壬基或环癸基,或者是双环烃基如十氢化萘环。 术语“3-20元杂环基”意指饱和的一价单环或双环烃环,其包含1-5个独立选自N、O 或S的杂原子,优选“3-10元杂环基”。术语“3-10元杂环基”意指饱和的一价单环或双环烃 环,其包含1-5个,优选1-3个选自N、O或S的杂原子。所述杂环基可以通过所述碳原子中的任 一个或氮原子(如果存在的话)与分子的其余部分连接。特别地,所述杂环基可以包括但不 限于:4元环,如氮杂环丁烷基、氧杂环丁烷基;5元环,如四氢呋喃基、二氧杂环戊烯基、吡咯 烷基、咪唑烷基、吡唑烷基、吡咯啉基;或6元环,如四氢吡喃基、哌啶基、吗啉基、二噻烷基、 硫代吗啉基、哌嗪基或三噻烷基;或7元环,如二氮杂环庚烷基。任选地,所述杂环基可以是 苯并稠合的。所述杂环基可以是双环的,例如但不限于5,5元环,如六氢环戊并[c]吡咯-2 (1H)-基环,或者5,6元双环,如六氢吡咯并[1,2-a]吡嗪-2(1H)-基环。含氮原子的环可以是 部分不饱和的,即它可以包含一个或多个双键,例如但不限于2,5-二氢-1H-吡咯基、4H-[1, 3,4]噻二嗪基、4,5-二氢噁唑基或4H-[1,4]噻嗪基,或者,它可以是苯并稠合的,例如但不 限于二氢异喹啉基。根据本发明,所述杂环基是无芳香性的。 术语“C6-20芳基”应理解为优选表示具有6~20个碳原子的一价芳香性或部分芳香 性的单环、双环或三环烃环,优选“C6-14芳基”。术语“C6-14芳基”应理解为优选表示具有6、7、 8、9、10、11、12、13或14个碳原子的一价芳香性或部分芳香性的单环、双环或三环烃环 (“C6-14芳基”),特别是具有6个碳原子的环(“C6芳基”),例如苯基;或联苯基,或者是具有9个 13 CN 111548359 A 说 明 书 8/10 页 碳原子的环(“C9芳基”),例如茚满基或茚基,或者是具有10个碳原子的环(“C10芳基”),例如 四氢化萘基、二氢萘基或萘基,或者是具有13个碳原子的环(“C13芳基”),例如芴基,或者是 具有14个碳原子的环(“C14芳基”),例如蒽基。 术语“5-20元杂芳基”应理解为包括这样的一价单环、双环或三环芳族环系:其具 有5~20个环原子且包含1-5个独立选自N、O或S的杂原子,例如“5-14元杂芳基”。术语“5-14 元杂芳基”应理解为包括这样的一价单环、双环或三环芳族环系:其具有5、6、7、8、9、10、11、 12、13或14个环原子,特别是5或6或9或10个碳原子,且其包含1-5个,优选1-3个彼此独立选 自N、O或S的杂原子并且,另外在每一种情况下可为苯并稠合的。特别地,杂芳基选自噻吩 基、呋喃基、吡咯基、噁唑基、噻唑基、咪唑基、吡唑基、异噁唑基、异噻唑基、噁二唑基、三唑 基、噻二唑基、噻-4H-吡唑基等以及它们的苯并衍生物,例如苯并呋喃基、苯并噻吩基、苯并 噁唑基、苯并异噁唑基、苯并咪唑基、苯并三唑基、吲唑基、吲哚基、异吲哚基等;或吡啶基、 哒嗪基、嘧啶基、吡嗪基、三嗪基等,以及它们的苯并衍生物,例如喹啉基、喹唑啉基、异喹啉 基等;或吖辛因基、吲嗪基、嘌呤基等以及它们的苯并衍生物;或噌啉基、酞嗪基、喹唑啉基、 喹喔啉基、萘啶基、蝶啶基、咔唑基、吖啶基、吩嗪基、吩噻嗪基、吩噁嗪基等。 除非另有说明,杂环基、杂芳基或亚杂芳基包括其所有可能的异构形式,例如其位 置异构体。因此,对于一些说明性的非限制性实例,吡啶基或亚吡啶基包括吡啶-2-基、亚吡 啶-2-基、吡啶-3-基、亚吡啶-3-基、吡啶-4-基和亚吡啶-4-基;噻吩基或亚噻吩基包括噻 吩-2-基、亚噻吩-2-基、噻吩-3-基和亚噻吩-3-基。 附图说明 图1为本发明实施例1制备的化合物2DQQT-Se和实施例2制备的化合物2DQQT-S的 紫外-可见吸收光谱。 图2为本发明实施例1制备的化合物2DQQT-Se和实施例2制备的化合物2DQQT-S的 循环伏安曲线。 图3为本发明实施例1制备的化合物2DQQT-Se和实施例2制备的化合物2DQQT-S的 电流-电压曲线。












