技术摘要:
本发明涉及体外诊断检测技术领域,特别是涉及一种25‑羟基维生素D检测试剂盒、制备方法及检测方法。一种25‑羟基维生素D检测试剂盒,包括:R1试剂、R2试剂、R3试剂及样本处理试剂,其中,所述R1试剂包括链霉亲和素磁微粒溶液;所述R2试剂包括碱性磷酸酶标记的25‑羟基 全部
背景技术:
维生素D是一种脂溶性固醇类衍生物,主要有维生素D2与D3两种形式。维生素D2由 紫外线照射植物中的麦角固醇产生;维生素D3则由人体表皮和真皮内含有的7-脱氢胆固醇 经日光中紫外线照射转变而成。在人体内,维生素D2和D3与血浆中维生素D结合蛋白结合并 转运到肝脏,经肝细胞微粒体中的单氧酶系统(25-羟化酶)的作用,形成25-羟基维生素D (包括25-羟基维生素D2和25-羟基维生素D3)。25-羟基维生素D在肾近端小管上皮细胞线粒 体内经α羟化酶系统作用下转变为1,25-二羟基维生素D,它是维生素D最大的生物作用形 式,可促进肠道钙结合蛋白的合成。而25-羟基维生素D是人体内维生素D代谢中的主要储存 形式,能够反映机体的维生素D水平,因此通过检测25-羟基维生素D来评估人体维生素D水 平。 维生素D是维持骨骼健康的主要元素,通过调节人体内的骨钙代谢和血磷代谢促 进人体内骨骼生长,还参与人体细胞的分化和免疫功能的调节,直接关系到人体新陈代谢 的平衡进而影响身体健康状况。维生素D缺乏将导致肌肉乏力,儿童期维生素D的严重缺乏 将导致骨骼畸形,即佝偻病;若该病发生于成人,则会出现发育成熟的骨骼钙化不全,成为 骨软化症。研究表明,维生素D缺乏可能使某些心血管疾病、自身免疫性疾病和感染疾病的 发病率升高,而长期摄入过多的维生素D,将引起高血钙和高尿钙,严重者将因肾钙化、心脏 和大动脉钙化而死亡。越来越多的医疗专业人员和患者已经意识到维生素D的缺乏或过量 均会对健康产生风险,医疗机构检验量激增,因此需要我们提供更稳定、准确的检测试剂, 帮助医生得到准确的检测结果。当然,25-羟基维生素D测定试剂的检测结果仅供临床参考, 不能单独作为诊断或排除病例的依据。 然而,目前采用的化学发光免疫法检测25-羟基维生素D,仍有灵敏度低、特异性 差、重现性差、检测范围窄等问题。仍需开发一种检验灵敏度高、特异性强、检测范围宽、重 现性好的25-羟基维生素D检测试剂。
技术实现要素:
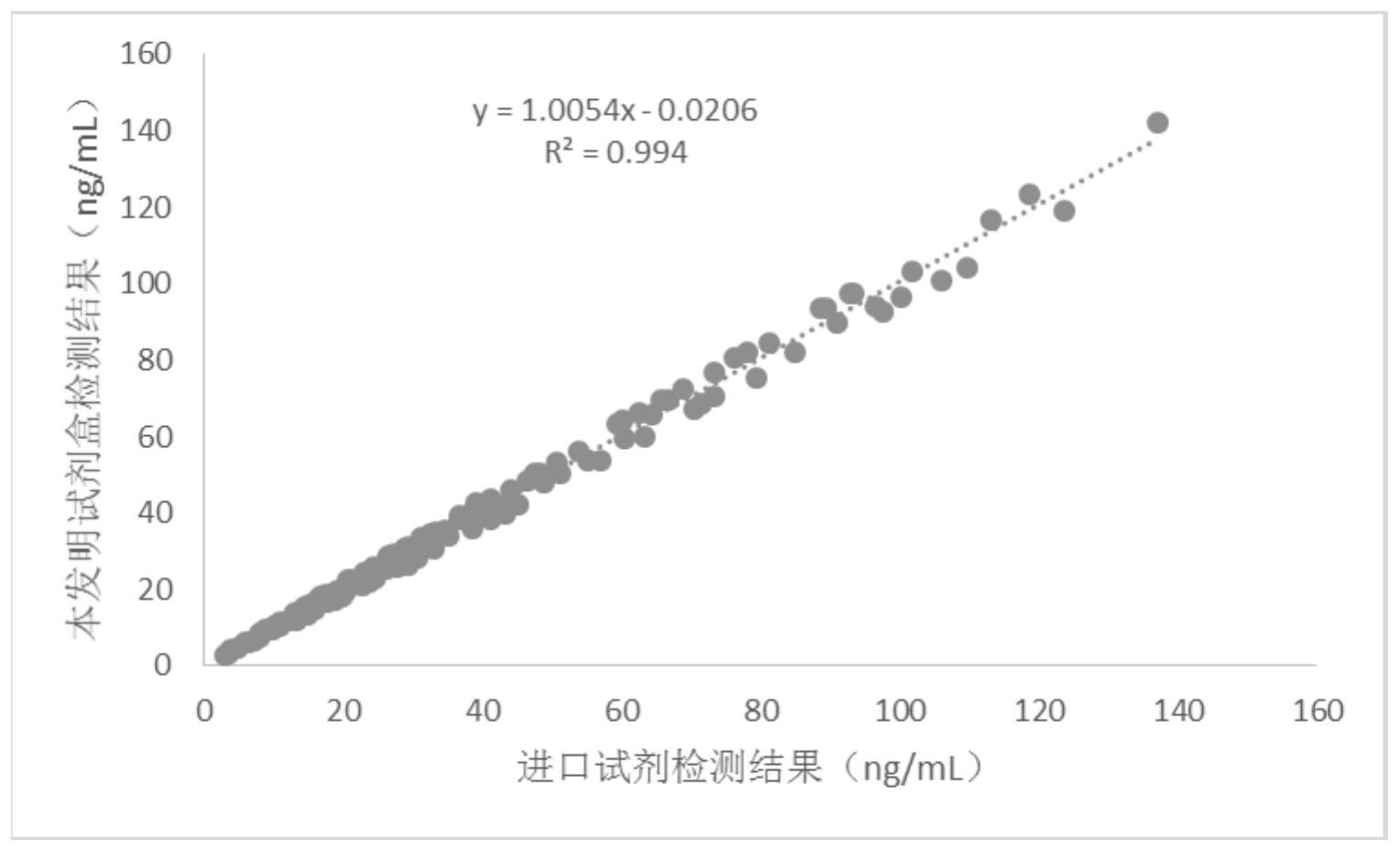
本发明的目的在于克服现有技术的缺陷,提供一种检验灵敏度高、特异性强、检测 范围宽、重现性好的25-羟基维生素D检测试剂盒、制备方法及检测方法。 为实现上述目的,本发明提供了一种25-羟基维生素D检测试剂盒,采取以下技术 方案: 一种25-羟基维生素D检测试剂盒,其特征在于,包括:R1试剂、R2试剂、R3试剂及样 本处理试剂,其中, 所述R1试剂包括链霉亲和素包被的磁微粒溶液,所述链霉亲和素包被的磁微粒的 5 CN 111721944 A 说 明 书 2/17 页 浓度为0.05~1mg/ml,所述磁微粒的粒径为1~4μm; 所述R2试剂包括碱性磷酸酶标记的25-羟基维生素D单克隆抗体溶液,所述碱性磷 酸酶标记的抗25-羟基维生素D单克隆抗体的浓度为0.2~1.0ng/mL,抗25-羟基维生素D单 克隆抗体与碱性磷酸酶的标记比例为1:1~10:1; 所述R3试剂包括生物素标记的25-羟基维生素D抗原,生物素标记的25-羟基维生 素D抗原浓度为0.05~0.2%; 所述样本处理试剂包括弱酸性缓冲液、还原剂及低级醇溶剂,用于从结合蛋白中 解离25-羟基维生素D。 本发明人通过大量研究实验考察后发现,传统技术中的待测样本中25-羟基维生 素D与碱性磷酸酶标记的25-羟基维生素D单克隆抗体往往结合不充分,使检测结果不准确、 试剂盒的灵敏度低。其中一个原因在于,待测样本常采用强碱性溶液使其中的25-羟基维生 素D解离出来,然而强碱性溶液在一定程度上会使碱性磷酸酶的活性降低,使得解离出来的 25-羟基维生素D没有与碱性磷酸酶标记的25-羟基维生素D单克隆抗体充分结合,导致检测 灵敏度低,检测结果不准确;另一个原因在于,25-羟基维生素D属于小分子疏水物质,不易 与碱性磷酸酶标记的25-羟基维生素D单克隆抗体结合,导致检测灵敏度低,检测结果不准 确。 在上述研究发现的基础上,本发明对传统技术进行了改进,将样本处理试剂采用 弱酸性缓冲液,使25-羟基维生素D从待测样本中有效解离的同时,保持碱性磷酸酶标记的 25-羟基维生素D单克隆抗体的活性;采用还原剂避免25-羟基维生素D转化,提高25-羟基维 生素D抗原活性,促进25-羟基维生素D与碱性磷酸酶标记的25-羟基维生素D单克隆抗体结 合;采用低级醇溶剂可促进25-羟基维生素D溶解。该样本处理试剂各成分协同作用能够使 25-羟基维生素D从待测样本中有效解离,并保持25-羟基维生素D与碱性磷酸酶标记的25- 羟基维生素D单克隆抗体的活性,并使二者充分结合,达到该检测试剂盒检测准确,灵敏度 高的效果。 在其中的一个实施例中,所述弱酸性缓冲液的pH值为5.5~6.9;所述弱酸性缓冲 液选自柠檬酸缓冲液、乙酸缓冲液或磷酸缓冲液中的一种;所述弱酸性缓冲液优选为柠檬 酸缓冲液;所述柠檬酸缓冲液的浓度为0.05~2.5%,优选为柠檬酸缓冲液的浓度为1.5%。 在其中的一个实施例中,所述还原剂选自二硫苏糖醇、三(2-羧乙基)膦盐酸盐,还 原性谷胱甘肽、半胱氨酸或β-巯基乙醇中的一种;所述还原剂优选为β-巯基乙醇,所述β-巯 基乙醇的浓度为0.05%~5%,优选为所述β-巯基乙醇的浓度为0.1%~2.5%;更优选为β- 巯基乙醇的浓度为0.25%~1%,最优选为β-巯基乙醇的浓度为0.5%; 在其中的一个实施例中,所述低级醇溶剂的浓度为10%~20%,优选为低级醇溶 剂的浓度为10%~15%,更优选为低级醇溶剂的浓度为15%;所述低级醇溶剂选自甲醇或 乙醇中的一种。 在其中的一个实施例中,所述样本处理试剂还包括0.02~0.1%的防腐剂,所述防 腐剂为叠氮化钠或Procline300中的一种。 在其中的一个实施例中,所述R1试剂还包括0.02~0.1mol/L的2-(N-吗啉)乙磺酸 缓冲液及0.02~0.1%的防腐剂,所述防腐剂为叠氮化钠或Procline300中的一种; 在其中的一个实施例中,所述R2试剂还包括0.02~0.1mol/L的2-(N-吗啉)乙磺酸 6 CN 111721944 A 说 明 书 3/17 页 缓冲液及0.02~0.1%的防腐剂,所述防腐剂为叠氮化钠或Procline300中的一种; 在其中的一个实施例中,所述R3试剂还包括0.02~0.1mol/L的2-(N-吗啉)乙磺酸 缓冲液及0.02~0.1%的防腐剂,所述防腐剂为叠氮化钠或Procline300中的一种。 在其中的一个实施例中,所述试剂盒还包括校准品及质控品,所述校准品和质控 品分别包括25-羟基维生素D抗原、血清、防腐剂和缓冲液,所述血清选自羊血清、牛血清、马 血清、驴血清或含人血清中的一种,所述防腐剂选自叠氮化钠和Procline300中的一种,所 述防腐剂的质量百分比浓度为0.02~0.1%,所述缓冲液选自PBS缓冲液、HEPES缓冲液、 Tris-Hcl缓冲液、MES缓冲液和MOPS缓冲液中的一种,所述缓冲液pH值为7.2~7.4;所述校 准品液系列中25羟基维生素D抗原浓度分别为0.0ng/mL、20ng/mL、40ng/mL、80ng/mL、 100ng/mL和120ng/mL;所述质控品液系列中25羟基维生素D抗原浓度分别为20ng/mL和 80ng/mL。 本发明还提供了一种如上所述的25-羟基维生素D检测试剂盒的制备方法,其特征 在于,包括R2试剂中碱性磷酸酶标记的抗25-羟基维生素D单克隆抗体的制备方法包括: (1)ALP-mal的制备: 1)添加DMF到EMCS中,配制成60~100mM的EMCS溶液; 2)将EMCS溶液添加到ALP调制用缓冲液中; 3)搅拌ALP溶液的同时添加上述混合液,温度35~38℃,加热50~70分钟; 4)进行离心脱盐,回收离心脱盐后溶液; (2)ALP-mal标记还原: 1)缓冲液置换,用离心脱盐柱进行25-羟基维生素D单克隆抗体缓冲液的置换,回 收缓冲液置换后的溶液; 2)凝胶过滤用缓冲液溶解MEA,配制0.2~0.5M的MEA溶液; 3)25-羟基维生素D单克隆抗体溶液的巯基化; 4)脱盐,反应结束后进行离心脱盐,回收脱盐后溶液; 5)ALP-mal的导入,将ALP-mal加入到上述溶液中,密封,2-8℃静置反应约16-24小 时; 6)终止,添加0.1M的MEA溶液到步骤5)中的溶液中,充分搅拌,温度35~38℃,反应 5~15分钟; 7)保存,终止后的溶液2-8℃环境下保存。 在其中的一个实施例中,所述25-羟基维生素D检测试剂盒,其特征在于,所述R3试 剂中生物素标记的抗25-羟基维生素D抗原的制备方法,包括如下步骤: (1)将所述25羟基维生素D抗原用脱盐柱中进行脱盐,得纯化液; (2)按照DMF:生物素=1:3~5的比例配制1~30mM生物素溶液; (3)将纯化液加入到生物素溶液中,常温反应20~40min; (4)反应后脱盐,回收离心液即可得到生物素标记的抗25羟基维生素D抗原。 在其中的一个实施例中,所述的25-羟基维生素D检测试剂盒的制备方法,其特征 在于,所述R1试剂中链霉素亲和素包被的磁微粒的制备方法包括如下步骤:取链霉亲和素 磁微粒溶液,用0.02~0.1mol/LTRIS缓冲溶液稀释得到的浓度为0.05~1mg/ml链霉亲和素 磁微粒。 7 CN 111721944 A 说 明 书 4/17 页 在其中的一个实施例中,所述的25-羟基维生素D检测试剂盒的制备方法,其特征 在于,所述校准品液系列和质控品液系列的制备方法为: (1)用缓冲液、血清和防腐剂配制成校准品稀释液; (2)用DMF溶解25-羟基维生素D抗原; (3)用步骤(1)中的校准品稀释液稀释溶解后的25羟基维生素D抗原,得25羟基维 生素D抗原浓度分别为0ng/mL、20ng/mL、40ng/mL、80ng/mL、100ng/mL和120ng/mL的校准品 液系列;或者,用步骤(1)中的校准品稀释液稀释溶解后的25羟基维生素D抗原,得25羟基维 生素D抗原浓度分别为20ng/mL和80ng/mL的质控品液系列。 本发明还提供了一种用于检测25-羟基维生素D的化学发光免疫方法,其特征在 于,采用权利要求1-9中任一项所述的试剂盒,包括以下步骤: 步骤A:将待测样本、样本处理试剂和R2试剂混合,36~38℃温育20~40分钟,使待 测样本中的25-羟基维生素D充分解离,并与碱性磷酸酶标记的25-羟基维生素D单克隆抗体 充分结合,洗涤; 步骤B:加入R1试剂和R3试剂,36~38℃温育5~15分钟,洗涤; 步骤C:加入化学发光底物,使其在酶的催化下,产生发光信号,由光量子阅读系统 接收,光电倍增管对反应所产生的光子数进行测量,软件根据光信号与Cutoff值自动计算 待测样本中的25-羟基维生素D含量; 所述化学发光底物为(3-(2-螺旋金刚烷)-4-甲氧基-4-(3-磷氧酰)-苯基-1,2-二 氧环乙烷,AMPPD。 与现有技术相比,本发明具有以下有益效果: (1)本发明的一种25-羟基维生素D的检测试剂盒,样本处理试剂包括弱酸性缓冲 剂、还原剂及低级醇溶剂,三者协同发挥作用,能够有效将25-羟基维生素D从待测样本中解 离出来,并增强25-羟基维生素D的抗原活性及溶解性,保持碱性磷酸酶标记的抗25-羟基维 生素D单克隆抗体的活性,使25-羟基维生素D与碱性磷酸酶标记的抗25-羟基维生素D单克 隆抗体充分结合,从而提高了检测灵敏度及检测的准确度。 (2)本发明的25-羟基维生素D的化学发光免疫方法,采用上述试剂盒,先加入待测 样本与样本处理试剂和R2试剂,温育,使待测样本中的25-羟基维生素D充分解离,并与碱性 磷酸酶标记的25-羟基维生素D单克隆抗体充分结合形成复合物,洗涤,再加入R1试剂链霉 亲和素标记的磁性微粒及R3试剂生物素标记的25-羟基维生素D抗原,该方法使25-羟基维 生素D与碱性磷酸酶标记的25-羟基维生素D单克隆抗体充分结合,再清洗,避免了待测25- 羟基维生素D的损失,再加入链霉亲和素磁微粒与生物素标记的25-羟基维生素D抗原,从而 提高了检测灵敏度。 (3)本发明的25-羟基维生素D化学发光检测试剂盒通过免疫发光竞争法实现化学 发光检测,该试剂盒具有较高的灵敏度、特异性和较宽的检测范围。 (4)本发明提供的25-羟基维生素D化学发光检测试剂盒只需要40μL血清或者血浆 就可以进行检测,患者体验好,有利于患者接受。 (5)本发明提供的25-羟基维生素D的测试剂盒可以与全自动化学发光分析仪联 用,实现了自动化监测,避免了人为操作导致的误差,提高了检测速度和检测效率。 (6)本发明提供的25-羟基维生素D化学发光检测试剂盒使用高质量抗体抗干扰能 8 CN 111721944 A 说 明 书 5/17 页 力强,检测范围完全涵盖现有临床检测需求,具有极强的市场推广潜力。 附图说明 为了更清楚地说明本申请实施例或现有技术中的技术方案,下面将对实施例中所 需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明中记载的一 些实施例,对于本领域普通技术人员来讲,还可以根据这些附图获得其他的附图。 图1为本申请实施例中25-羟基维生素D检测试剂盒与进口试剂盒测定值得相关 性.。












