技术摘要:
本发明公开了一种用于乙肝治疗的纳米颗粒及其制备方法和治疗性疫苗。所述纳米颗粒包含HBsAg或HBcAg蛋白、免疫佐剂CpG、阳离子聚合物和阴离子聚合物。本发明提供了同时包裹HBsAg和免疫佐剂的纳米颗粒,以及同时包裹HBcAg和免疫佐剂的纳米颗粒,其形态规则、外形圆整、表 全部
背景技术:
乙型肝炎病毒(HBV)感染是世界上最常见的慢性病毒感染,全世界大约20亿人感 染了乙型肝炎病毒,其中有3.5亿人成为慢性乙肝携带者。在慢性乙肝感染过程中,会引起 肝脏低程度的炎症,同时伴随短暂的高程度的炎症发生和肝纤维化的激活,从而引发肝纤 维化和肝硬化的发生,最终导致代偿性肝脏疾病和肝细胞癌的发生。慢性乙肝感染在全球 多个地区流行,西太平洋和非洲的情况尤为严重。早在2010年的全球疾病负担研究中,HBV 感染已经是世界上最重要的公共卫生问题之一,是引起死亡的第十大疾病,全球每年大约 有78万人死于HBV感染。尽管现在的HBV预防疫苗,可以安全有效地阻断HBV传播,早在2015 时,WHO估计全球仍有2.6亿乙肝病毒携带者,相当于全球人口的3.5%。这些人大多都是在 HBV疫苗问世前出生的,所以慢性HBV感染仍然是严重的公共健康问题。 现在临床上主要有两类药物治疗慢性乙肝:一种是IFN-a,一方面它可以激活干扰 素刺激基因,产生抗病毒蛋白,在病毒复制的各个阶段,发挥抗病毒作用;另一方面,IFN-α 具有免疫调节作用,通过促进NK细胞、CD8 T细胞的胞毒作用等细胞介导的免疫反应,直接 发挥抗病毒作用。另一种是核苷类似物,主要是通过抑制HBV RNA逆转录形成HBV DNA,发挥 抗病毒作用。但是这两类药物又有明显的缺陷性:干扰素虽然可以完全清除HBV,但是它会 引起流感样症状、骨髓抑制、抑郁、疲劳等副作用,很多病人不能承受这些严重的副作用,从 而限制了IFN-a在临床上的应用。核苷类似物,它只能够抑制HBV DNA的复制,不能清除HBV, 而且核苷类似物需要病人长期服用。长期服用核苷类似物,一方面会使病毒发生变异,产生 耐药性;另一方面,会使病人产生严重的经济负担。 目前研究中的乙肝治疗性疫苗,主要有乙肝表面抗原(HBsAg)疫苗、乙肝表面抗 原-乙肝表面抗体复合物疫苗、乙肝表面抗原-乙肝核心抗原疫苗、乙肝表面抗原表位疫苗 和乙肝DNA疫苗等,这些研究中的疫苗都是使用铝佐剂、皂苷等传统佐剂,它们可以激活一 定的体液免疫,却不能有效地激活细胞免疫。然而细胞免疫对于HBV的清除发挥十分重要的 作用,因此这些目前研究中的乙肝治疗性疫苗,在临床试验中都没有达到理想的治疗效果。 专利CN 105288613 A公开了一种含重组乙肝表面抗原的纳米颗粒疫苗,其免疫活性依然有 待提高,且纳米颗粒的粒径较大,在抗原呈递方面还有待提高;另外其制备过程复杂,且过 程中使用有机溶剂,容易带来安全问题。
技术实现要素:
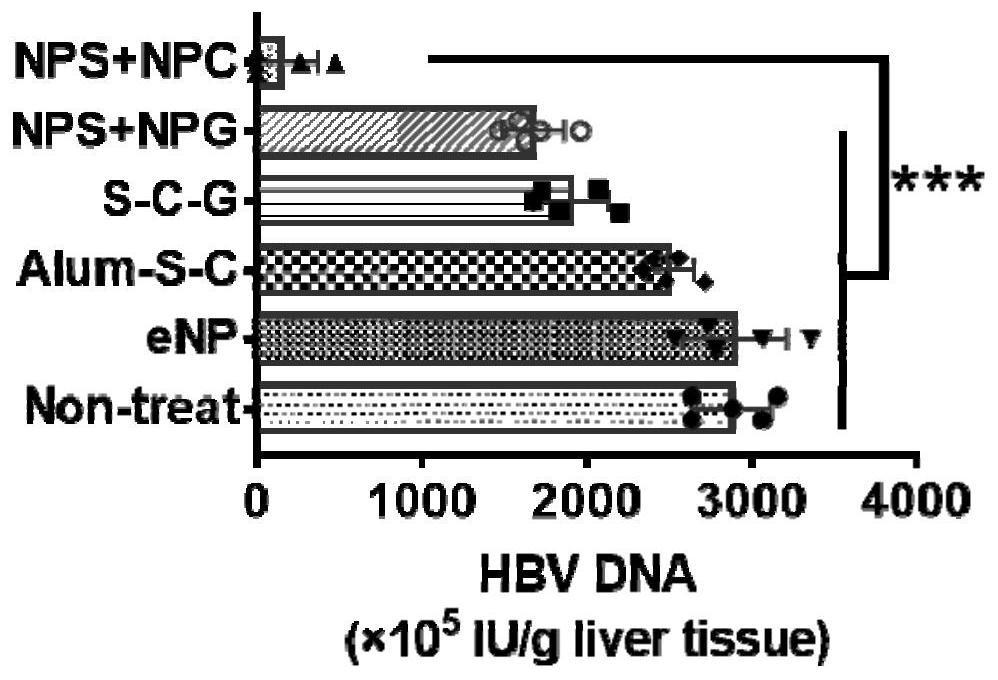
本发明的目的在于克服现有技术中存在的上述缺陷和不足,提供一种用于乙肝治 疗的纳米颗粒。 本发明的另一目的在于提供所述的用于乙肝治疗的纳米颗粒的制备方法。 3 CN 111728955 A 说 明 书 2/11 页 本发明的再一目的在于提供一种新型乙肝治疗性纳米疫苗。 本发明的上述目的是通过以下技术方案给予实现的: 一种乙肝治疗性纳米颗粒,包含HBsAg或HBcAg蛋白、免疫佐剂CpG、阳离子聚合物 和阴离子聚合物。 本发明首先分别提供两种包含HBcAg和CpG的纳米颗粒或包含HBsAg和CpG的纳米 颗。乙肝表面抗原(HBsAg)是位于乙肝病毒外膜上的一种蛋白,是一个广泛认可的具有免疫 原性的HBV抗原,宿主中和抗体的重要作用位点,也是疫苗设计的关键靶点,已经作为抗原 用于乙肝预防性疫苗中。乙肝核心抗原是位于乙肝病毒核心中的一种蛋白,能引起显著的T 细胞和B细胞应答,具有佐剂作用。CpG ODN是一种细菌来源的非甲基化的核苷酸序列,可以 与抗原呈递细胞(APCs)中的Toll样受体结合,促进APC细胞的成熟和活化,进而增强免疫反 应。本发明两种包含HBcAg和CpG的纳米颗粒和包含HBsAg和CpG的纳米颗粒,其粒径在50~ 200nm,更容易被抗原呈递细胞(APCs)捕获并向T细胞呈递抗原,促使T细胞和B细胞成熟活 化,增强免疫效果。本发明设计了同时包裹HBsAg和免疫佐剂的纳米颗粒,以及同时包裹 HBcAg和免疫佐剂的纳米颗粒,将这两种纳米颗粒共同使用,作为HBV治疗性纳米疫苗,可以 打破免疫耐受、激活免疫反应、清除HBV,实现慢性乙肝的治愈。 具体地,所述纳米颗粒为核壳结构,核为HBsAg或HBcAg蛋白与免疫佐剂,壳为阳离 子聚合物和阴离子聚合物。优选地,所述HBsAg蛋白的氨基酸序列如SEQ ID NO:1所示。 优选地,所述HBcAg蛋白的氨基酸序列如SEQ ID NO:2所示。 优选地,所述免疫佐剂为CpG,其核苷酸序列如SEQ ID NO:3所示。 优选地,所述阳离子聚合物为PEI(聚醚酰亚胺)、聚赖氨酸或壳聚糖中的一种或多 种。 进一步优选地,所述阳离子聚合物为壳聚糖。 优选地,所述阴离子聚合物为肝素、TPP(硫胺素焦磷酸)或透明质酸中的一种或多 种。 优选地,所述纳米颗粒的粒径为50~200nm,例如50~70nm、70~90nm、90~111nm、 110~130nm、130~150nm、150~170nm或170nm~200nm。 优选地,所述纳米颗粒的Zeta电位为 18至 30mV,例如 18至 20mV、 20至 22mV、 22至 24mV、 24至 26mV、 26至 28mV或 28至 30mV。 优选地,所述HBsAg或HBcAg蛋白的包封率为60%~90%,例如60%~65%,65%~ 70%,70%~75%、75%~80%、80%~85%或85%~90%。 优选地,所述免疫佐剂的包封率为65%~95%,例如65%~70%,70%~75%、 75%~80%、80%~85%、85%~90%或90%~95%。 优选地,制备纳米颗粒时,所述HBsAg或HBcAg蛋白:免疫佐剂:阳离子聚合物:阴离 子聚合物的质量比为1~3:10~15:40~50:25~35。 进一步优选地,所述HBsAg或HBcAg蛋白:免疫佐剂:阳离子聚合物:阴离子聚合物 的质量比为1:1.2:45:30 本发明还提供所述的乙肝治疗性纳米颗粒的制备方法,包括如下步骤: S1.提供包含阳离子聚合物的溶液、包含阴离子聚合物的溶液、包含HBsAg或HBcAg 蛋白的溶液和包含免疫佐剂的溶液; 4 CN 111728955 A 说 明 书 3/11 页 S2.使包含阳离子聚合物的溶液、包含阴离子聚合物的溶液、包含HBsAg或HBcAg蛋 白的溶液和包含免疫佐剂的溶液分别通过第1通道、第2通道、第3通道和第4通道到达混合 区域中,进行混合,得混合液; S3.将混合液过滤,浓缩,即得纳米颗粒。 优选地,所述包含阳离子聚合物的溶液、包含阴离子聚合物的溶液、包含HBsAg或 HBcAg蛋白的溶液和包含免疫佐剂的溶液的浓度比为0.4~0.6mg/mL:0.1~0.5mg/mL:5~ 20μg/mL:5~20μg/mL。 进一步优选地,所述包含阳离子聚合物的溶液、包含阴离子聚合物的溶液、包含 HBsAg或HBcAg蛋白的溶液和包含免疫佐剂的溶液的浓度比为0.45mg/mL:0.3mg/mL:10μg/ mL:12μg/mL。 优选地,包含阳离子聚合物的溶液、包含阴离子聚合物的溶液、包含HBsAg或HBcAg 蛋白的溶液和包含免疫佐剂的溶液在通道中都以匀速流动。 优选地,包含阳离子聚合物的溶液、包含阴离子聚合物的溶液、包含HBsAg或HBcAg 蛋白的溶液和包含免疫佐剂的溶液在通道中的流速相同。 进一步优选地,所述流速为1~20mL/min,例如1~5mL/min、5~10mL/min10~ 15mL/min或15~20mL/min。 在rAAV-1 .3HBV建立的慢性乙肝小鼠模型中,本发明制备的这两种纳米颗粒联合 使用,共同经足底皮下注射后,能产生强烈的免疫效果,可以打破免疫耐受,产生高滴度的 乙肝表面抗体(HBsAb),引起特异的针对HBsAg的细胞毒T淋巴细胞反应,有效清除血液和肝 脏中的HBV,具有非常显著的协同增效。因此,本发明还提供一种免疫原性组合物,包含上述 两种用于乙肝治疗的纳米颗粒。即上述包含HBsAg的纳米颗粒和包含HBcAg蛋白的纳米颗 粒。 优选地,还包含药学上可接受的辅料。 进一步优选地,所述免疫原性组合物为疫苗。 与现有技术相比,本发明具有以下有益效果: 本发明提供了同时包裹HBsAg和免疫佐剂的纳米颗粒,以及同时包裹HBcAg和免疫 佐剂的纳米颗粒,其形态规则、外形圆整、表面光滑、分散性好、粒径均一、包封率高、无明显 粘连、破损、坍塌等现象,通过采用CpG免疫佐剂,同时纳米颗粒粒径小,具有更强的免疫活 性;且纳米颗粒制备过程简单,不涉及有机溶剂,更安全环保,易于产业化。在rAAV-1.3HBV 建立的慢性乙肝小鼠模型中,本发明制备的这两种纳米颗粒混合联用,共同经足底皮下注 射后,能产生强烈的免疫效果,可以打破免疫耐受,产生高滴度的乙肝表面抗体(HBsAb),引 起特异的针对HBsAg的细胞毒T淋巴细胞反应,有效清除血液和肝脏中的HBV,效果显著优于 单独使用其中一种纳米颗粒及游离HBsAg HBcAg CpG的免疫效果。 附图说明 图1为本发明chitosan-HBsAg-CpG-heparin纳米颗粒制备的示意图。 图2为本发明chitosan-HBcAg-CpG-heparin纳米颗粒制备的示意图。 图3为本发明chitosan-CpG-heparin纳米颗粒制备的示意图。 图4为本发明实施实例1中chitosan-HBsAg-CpG-heparin纳米颗粒的透射电镜图。 5 CN 111728955 A 说 明 书 4/11 页 图5为本发明实施实例1中chitosan-HBcAg-CpG-heparin纳米颗粒的透射电镜图。 图6为本发明实施实例1中chitosan-HBsAg-CpG-heparin纳米颗粒的粒径分布图。 图7为本发明实施实例1中chitosan-HBcAg-CpG-heparin纳米颗粒的粒径分布图。 图8为本发明实施实例1中chitosan-CpG-heparin纳米颗粒的粒径分布图。 图9为本发明实施实例2中chitosan-HBsAg-CpG-heparin纳米颗粒的粒径分布图。 图10为本发明实施实例2中chitosan-HBcAg-CpG-heparin纳米颗粒的粒径分布 图。 图11为本发明实施实例3中chitosan-HBsAg-CpG-heparin纳米颗粒的粒径分布 图。 图12为本发明实施实例3中chitosan-HBcAg-CpG-heparin纳米颗粒的粒径分布 图。 图13为免疫后血清中HBsAg的浓度。 图14为末次免疫2周后血清中HBsAb的浓度。 图15为末次免疫2周后血清中IFN-γ滴度。 图16为末次免疫2周后产生HBsAb的脾细胞的数目。 图17为末次免疫2周后血清中HBV DNA的拷贝数。 图18为末次免疫2周后肝脏中HBV DNA的拷贝数。












