技术摘要:
本公开涉及用于量化生物组织的生物标志物的方法和系统。从以使得至少两个光谱子区间中的图像数据的组合与感兴趣的临床变量相关联的方式,使用成像传感器在主波长区间内的离散波长处获取的组织的多个图像确定两个光谱子区间。使用具有在至少两个光谱子区间内的波长的一 全部
背景技术:
成像技术通常用于帮助检测和诊断各种疾病。考虑到检测异常,分析受试者的生 物组织的图像以量化他们的生理参数。检测淀粉样蛋白和其它异常的常用技术包括正电子 发射断层摄影术(PET)扫描。PET扫描是昂贵的、耗时的,并且可能导致受试者的不适。 例如,患者视网膜中异常淀粉样蛋白的存在可用于诊断视网膜的状况。特别地,已 经示出,受试者视网膜中淀粉样蛋白的存在可以指示阿尔茨海默病的发作。还提出了其他 疾病的诊断,例如青光眼、糖尿病、糖尿病性视网膜病、高血压、心血管疾病、脑血管疾病、黄 斑变性、帕金森病、其他淀粉样病变和其他蛋白病可以基于对受试者视网膜内异常的检测。 最近,已经提出了涉及眼睛的高光谱图像的视觉分析和数字图像处理两者的技 术,以检测根源在于受试者的其他器官的疾病的表现。 基于生物组织的高光谱图像,特别是眼睛的图像的生物标志物的定量分析是用于 诊断若干健康状况的非常有前景的工具。然而,用于获取高光谱图像的商业系统仍然非常 昂贵且不易访问。
技术实现要素:
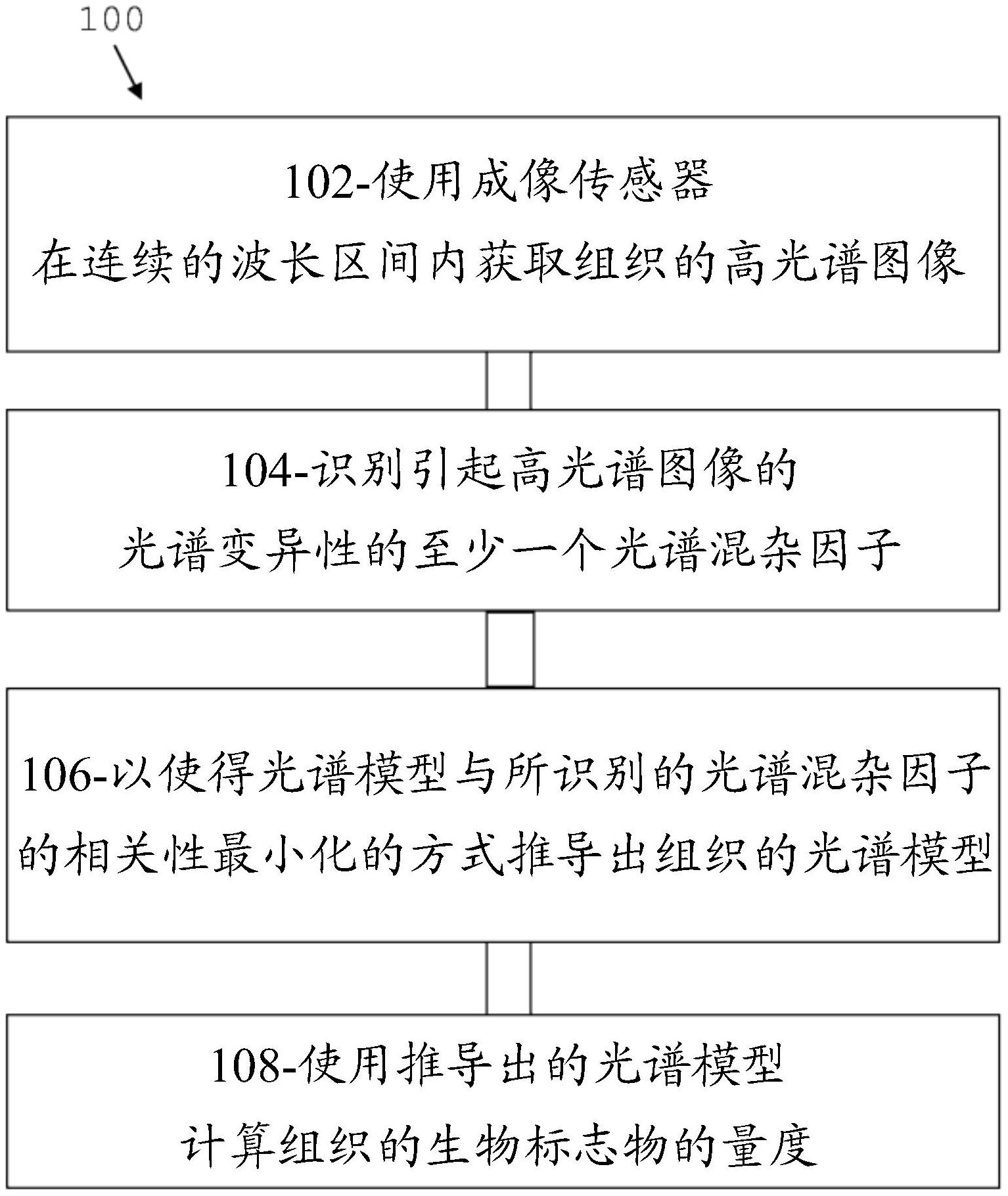
本发明的实施例提供了使用成像和图像数据处理算法来量化组织的生物标志物 的技术。特别地,本发明的各方面提供了获取和处理来自生物组织的高光谱图像数据并量 化与疾病相关联的组织中的生物标志物的系统和方法。本发明的另外各方面提供了从组织 获取多光谱图像数据并处理图像数据以量化生物标志物的系统和方法。 根据第一方面,本发明提供了一种用于量化组织的生物标志物的方法,所述方法 包括: 使用成像传感器在主波长区间内的离散波长处获取组织的多个图像; 使用处理器以使得至少两个光谱子区间中的图像数据的组合与感兴趣的临床变 量相关的方式确定至少两个光谱子区间;以及 利用处理器使用至少两个光谱子区间中的图像数据来计算组织的生物标志物的 量度; 其中,主波长区间比至少两个光谱子区间中的每个都宽,且引起所获取的图像的 光谱变异性的至少一个光谱混杂因子存在于组织中。 根据第二方面,本发明提供了一种用于量化组织的生物标志物的方法,所述方法 包括: 使用处理器从以使得至少两个光谱子区间中的图像数据的组合与感兴趣的临床 变量相关的方式,使用成像传感器在主波长区间内的离散波长处获取的组织的多个图像, 6 CN 111587365 A 说 明 书 2/15 页 确定至少两个光谱子区间; 使用具有在至少两个光谱子区间内的波长的一个或更多个光源照射组织; 使用成像传感器获取由组织反射的光的测量结果;以及 使用所获取的测量结果来计算组织的生物标志物的量度; 其中,主波长区间比至少两个光谱子区间中的每个都宽,且引起所获取的图像的 光谱变异性的至少一个光谱混杂因子存在于组织中。 在实施例中,感兴趣的临床变量包括疾病、疾病的严重性或亚型、已知的生物标志 物或生理状态中的任一种或组合。 在实施例中,主波长区间使得所获取的图像表示组织的高光谱或多光谱表示。 在实施例中,该方法包括获取多个图像,包括使用在不同波长处操作的一个或更 多个相机。 在实施例中,该方法包括提取至少两个光谱子区间中的每一个的光谱参数以形成 组织的多光谱表示。 在实施例中,该方法包括识别引起所获取的图像中的光谱变异性的至少一个光谱 混杂因子。 在实施例中,确定至少两个光谱子区间是以使得至少两个光谱子区间的组合的光 谱信息与光谱混杂因子是正交的、不相关的或独立的方式来执行的。 在实施例中,确定至少两个光谱子区间是通过应用频带选择方法、机器学习算法 或人工智能引擎来执行的。 在实施例中,感兴趣的变量包括使用正电子发射断层摄影术(PET)在脑中测量的 或在脑脊液(CSF)中测量的β淀粉样蛋白的量或分布。 在实施例中,确定至少两个光谱子区间包括使用多变量统计、机器学习或人工智 能技术。 在实施例中,使用多变量统计、机器学习或人工智能技术计算生物标志物的量度。 在实施例中,多变量统计包括回归、逻辑回归或判别 在实施例中,机器学习或人工智能技术考虑图像数据中的人口统计信息、临床信 息、其它感兴趣的变量或多个感兴趣的区域。 在实施例中,确定至少两个光谱子区间是由机器学习算法执行的,该机器学习算 法将多光谱数据变换成表示生物标志物的评分。 在实施例中,该方法包括将光学滤波器应用于一个或更多个光源。 在实施例中,该方法包括沿着由一个或更多个光源产生的光的光路应用光学滤波 器。 在实施例中,组织是人的视网膜,且光学滤波器被嵌入在施加于人的眼睛上的隐 形眼镜片内。 根据第二方面,本发明提供了一种用于量化组织的生物标志物的系统,该系统包 括: 光学组件,所述光学组件包括一个或更多个光源,所述光学组件被布置成以至少 两个预定的光谱区间内的波长照射组织的一部分;以及 成像组件,所述成像组件包括成像传感器,所述成像传感器被布置成接收从组织 7 CN 111587365 A 说 明 书 3/15 页 的部分反射的光并将所述光转换成数字数据; 其中至少两个预定的光谱子区间是已知的感兴趣的变量所特有的。 在实施例中,该系统包括生物标志物选择组件,所述生物标志物选择组件被布置 成基于用户所选择的组织的生物标志物选择至少两个光谱区间。 在实施例中,该系统包括处理模块,所述处理模块被布置成从成像传感器接收数 据,并且所述处理模块被配置为: 结合并处理从成像传感器接收的数据以提取光谱信息并形成组织的多光谱表示; 以及 处理组织的多光谱表示以量化生物标志物。 在实施例中,组织为视网膜的一部分,生物标志物是用于预测/分级风险、筛查或 诊断阿尔茨海默病的β淀粉样蛋白(AB)的量度,至少两个光谱区间包括位于475nm中的约 100nm内、545nm中的约100nm内和725nm中的约100nm内的三个波段,每个波段均具有低于约 200nm的带宽。 在实施例中,光学组件被布置成产生具有在至少两个光谱区间内的光谱的光。 在实施例中,照明组件包括光学滤波器,所述光学滤波器被布置成在至少两个子 光谱区间内对所生成的光路或反射光路进行滤波。 在一个实施例中,组织是视网膜的一部分,感兴趣的变量是与阿尔茨海默病相关 的脑或脑脊液的β淀粉样蛋白水平,至少两个光谱区间包括位于475nm的约100nm内、545nm 的约100nm内和725nm的约100nm内的三个波段,且每个波段均具有低于约200nm的带宽。 根据第三方面,本发明提供了一种用于量化组织的生物标志物的方法,所述方法 包括: 使用成像传感器在连续波长区间内获取组织的高光谱图像; 识别引起高光谱图像的光谱变异性的至少一个光谱混杂因子; 以使得光谱模型与所识别的光谱混杂因子的相关性最小化的方式来推导出组织 的光谱模型;以及 使用所推导出的光谱模型来计算组织的生物标志物的量度。 在实施例中,组织的光谱模型被推导为与所识别的光谱混杂因子正交、不相关或 独立。 在实施例中,光谱模型是从两个组之间的主光谱差异推导出的,每个组具有不同 量的感兴趣的变量。 在实施例中,推导出组织的光谱模型包括通过以使得组织的干净高光谱表示具有 由至少一个光谱混杂因子的光谱特征所引起的减小的变异性的方式处理组织的高光谱表 示和至少一个光谱混杂因子的光谱特征来推导出组织的干净高光谱表示。 在实施例中,获取组织的高光谱图像包括使用一个或更多个光源,利用在连续的 预定的波长范围内的单色或窄带宽光,顺序地照射组织,且对于每个波长,使用成像传感器 来获取由组织反射的光的测量结果。 在实施例中,识别至少一个光谱混杂因子包括从光谱数据库读取光谱混杂因子的 一个或更多个光谱曲线并处理来自高光谱图像的光谱信息以及一个或更多个光谱曲线。 在实施例中,推导出干净高光谱表示包括从光谱信息中去除由至少一个光谱混杂 8 CN 111587365 A 说 明 书 4/15 页 因子的光谱曲线引起的光谱变异性。 在实施例中,识别至少一个光谱混杂因子包括使用特定的光谱混杂因子作为参考 混杂因子并计算Δ高光谱图像,该Δ高光谱图像表示两个高光谱图像之间的逐像素和逐波 长的差值。 在实施例中,根据以下步骤处理光谱信息: 计算在感兴趣的变量方面不同的组之间的组间光谱变异性; 提取组内光谱数据库的第一主特征向量集;以及 使用正交投影去除一个或更多个特征向量以产生中间数据集,在所述中间数据集 中组内变异性基本上被去除; 其中,生物标志物是基于组织的干净光谱表示使用光谱维数减小来量化的。 在实施例中,根据以下步骤处理光谱信息: 计算光谱数据库的不同组之间的组间光谱变异性; 提取不同组之间的组间变异性的第一主特征向量集; 使用基于第一主特征向量集的正交投影从不同组的组合去除组间变异性以产生 中间数据集,在所述中间数据集中组间变异性基本上被去除; 计算中间数据集内的组内变异性;提取中间数据集的组内变异性的第二主特征向 量集;以及 提取统计数据库中的多个干净光谱表示的第三主特征向量集; 其中,从临时光谱信息中去除由至少一个非特异性混杂因子引起的光谱变异性包 括使用基于第二主特征向量集的正交投影从临时光谱信息中去除组内变异性以创建组织 的干净光谱表示;以及 其中,使用基于组织的干净光谱表示上的第三主特征向量集的投影来量化生物标 志物。 在实施例中,至少一个光谱混杂因子包括至少一个眼部混杂因子,并且量化的生 物标志物指示人的视网膜中存在或不存在感兴趣的变量。 在实施例中,至少一个眼部光谱混杂因子包括黑色素含量、白内障、晶状体变色、 血红蛋白含量、视网膜病、视网膜色素上皮厚度或密度、RNFL厚度、脉络膜厚度、黄斑色素含 量和/或其组合的变化。 根据第五方面,本发明提供了一种用于量化组织的生物标志物的系统,所述系统 包括: 照明组件,所述照明组件被布置成利用连续波长范围内的单色或窄带宽光依次照 射组织的一部分; 成像组件,所述成像组件包括成像传感器,所述成像传感器被布置成接收由组织 的部分反射的光并将所述光转换成数字数据;以及 处理模块与存储模块,所述处理模块与存储模块被布置成从成像传感器接收数据 并被配置成执行指令以执行根据第四方面的方法。 本发明适用于任何测量指示疾病状态或疾病倾向的任何生物标志物。示例包括但 不限于用于阿尔茨海默病的β淀粉样蛋白、受试者的以及受试者之间的视网膜(眼内和两眼 之间)中白内障和黑色素含量的变化水平、以及通过PET扫描测量的脑中的β淀粉样蛋白、或 9 CN 111587365 A 说 明 书 5/15 页 脑脊液中的β淀粉样蛋白、RNFL厚度、视网膜厚度、视网膜内或视网膜下方血液。 通过阅读以下仅参照附图以示例方式给出的对说明性实施例的非限制性描述,前 述和其它特征将变得更加明显。 附图说明 将仅参考附图通过示例的方式来描述本公开的实施例,其中: 图1示出了具有用于基于高光谱成像来量化组织的生物标志物的方法步骤的流程 图; 图2示出了从白内障和色素沉着去除光谱效应之前和之后的光谱数据; 图3和10示出了用于量化组织的生物标志物的系统的示意图; 图4示出了四只眼睛的代表性HS蒙太奇,其示出了由于视网膜和脉络膜脉管系统、 眼部色素和眼部介质透明度(A-D)而导致的具有阳性脑β淀粉样蛋白PET扫描(阿尔茨海默 病)的个体的固有变异性和不具有眼内和眼间数据的个体(PET阴性对照)的固有变异性;采 样的中央凹位置,具有主内视网膜血管的分割的颞血管弧的上方和下方(E)和在对照和病 例的不同采样位置处的归一化反射光谱(F到K); 图5示出了来自具有阳性脑β淀粉样蛋白PET扫描(阿尔茨海默病)的个体和不具有 阳性脑β淀粉样蛋白PET扫描的个体(PET阴性对照)的视网膜成像数据的两种主光谱混杂因 子的估计曲线图。(A)示出了在指定的采样位置(B)处的校正的反射光谱曲线图,(C)示出了 使用用于所有波长的显著性的错误发现率控制的组之间的双侧未配对t检验的P值的曲线 图,以及在对应于两组之间的主光谱差异的指定采样位置处的光谱模型的曲线图(D); 图6示出了描述在不同采样位置处使用HS评分的具有阳性脑β淀粉样蛋白PET扫描 (阿尔茨海默病)的个体和不具有阳性脑β淀粉样蛋白PET扫描的个体(PET阴性对照)之间的 区别的曲线图; 图7示出了描述在验证数据集中HS评分如何能够区分具有阳性脑β淀粉样蛋白PET 扫描(阿尔茨海默病)的个体和不具有阳性脑β淀粉样蛋白PET扫描的个体(PET阴性对照)的 曲线图。 图8,在(A)中示出了研究眼和对侧眼的HS评分之间的相关性,以及在(B)中示出了 白内障手术前的HS评分和白内障手术后的HS评分之间的相关性; 图9示出了具有用于基于多光谱成像来量化生物组织的生物标志物的方法步骤的 流程图; 图10示出了用于基于多光谱成像来量化生物组织的生物标志物的系统的示意图; 图11示出了在眼底相机的光学光路中的不同位置处具有带通滤波器的视网膜多 光谱成像的示意图,该眼底相机具有宽带光源和在成像传感器处具有传统颜色阵列; 图12示出了使用光源和在成像传感器处的定制与修改的滤波器阵列的视网膜多 光谱成像的示意图; 图13示出了在成像传感器处使用具有相对窄的光带和传统颜色阵列的照明的视 网膜多光谱成像的示意图; 图14示出了使用具有相对窄的频带的顺序波段照明和成像传感器的视网膜多光 谱成像的示意图; 10 CN 111587365 A 说 明 书 6/15 页 图15示出了用于阿尔茨海默病的视网膜多光谱成像的三个波段的选择。ADSF示出 了在针对检测视网膜中的淀粉样蛋白的情况下使用哪些波段(滤波器1、2、3); 图16示出了用具有阳性脑β淀粉样蛋白PET扫描(阿尔茨海默病)的个体和不具有 阳性脑β淀粉样蛋白PET扫描的个体(PET阴性对照)的高光谱(HS)和多光谱(MS)视网膜成像 获得的评分之间的关联; 图17示出了与常规颜色(RGB)图像(左)相比,分别来自两个青光眼患者的MS评分 图像(右)的对比增强的表示(A和B),以及在来自常规照片的每个单独RGB颜色通道的评分、 来自RGB眼底图像的评分与来自MS图像的评分之间实现的对比增强的比较(C); 图18示出了通过OCT测量的视网膜神经纤维层(RNFL)厚度的图像(A)、使用具有三 个光谱区间的MS成像估计的RNFL厚度的图像(B)以及示出了通过OCT测量的RNFL厚度与使 用MS成像估计的厚度之间的相关性的曲线图(C); 图19示出了如(A)中所示的传统RGB眼底图像上难以检测视网膜下的和视网膜内 的液体。使用MS成像(B),液体是清楚明显的; 图20示出了脉络膜新生血管(CNV)通常难以用如(A)中所示的传统RGB眼底成像检 测。使用MS成像(B)CNV更明显;以及 图21是描绘基于视网膜MS图像的年龄预测的曲线图。












