技术摘要:
拓扑异构酶I抑制剂通过在原位经历β消除的接头与大分子连接的偶联物,联合携癌对象中一种或多种经评估的DNA损伤反应(DDR)缺陷,细胞周期检查点抑制剂和/或DDR抑制剂,为携癌对象提供改善的结果。
背景技术:
已知拓扑异构酶I抑制剂用于治疗各种癌症,因为它们是拓扑异构酶I催化的必需 连接步骤的抑制剂,该连接步骤用于解决DNA复制超卷积导致的张力释放造成的单链DNA损 伤(DNA复制需要拓扑异构酶I)。拓扑异构酶I抑制剂包括喜树碱及其类似物。许多这样的化 合物已被证明和用于治疗各种癌症的化疗。 在具有一些基因缺陷的癌细胞中,已观察到施用拓扑异构酶I抑制剂比起不具有 这样的缺陷的癌细胞效力增强。例如,在具有哺乳动物肿瘤的BRCA1-缺陷型小鼠中施用一 种拓扑异构酶抑制剂SN-38和聚乙二醇的偶联物,不仅BRCA1缺陷和SN-38对拓扑异构酶的 抑制组合有效,而且还克服了ABCG2介导的抗性。见例如Zander,S.A.L.等,PLOS One(2012) 7:e45248。此外,已联合施用各种拓扑异构酶抑制剂和额外的作为DDR抑制剂和/或细胞周 期检查点抑制剂的抗癌药。见例如Abal,M.等,Oncol.Gene(2004)23:1737-1744,Wainberg, Z.A.等,Targ Oncol.(2017)12:775-785;Verschraegen,C.F.等,Cancer(2013)5:418-429; 和Gray ,J .等,Cancer Biol .and Ther .(2012)13:614-622;Josse ,R e .al ,Cancer Res (2014)74:6968-6978;Ma,C.X.等,Breast Cancer Res Treat(2013)137:483-492。体外研 究也显示抑制Werner综合征解旋酶(WRN)(DNA复制和修复中重要的蛋白质)的表达增强伊 立替康对癌细胞的作用。见Futami,K.等,Biol Pharm Bull(2007)30:1958-1961。也在临床 实验中测试了细胞检查点抑制剂和各种DNA损伤药物的组合。(见Visconti ,R .等 , J.Exp.Clin.Cancer Res.(2016)35:153.) 此外,对于不同基因和基因组位置上DNA损伤反应缺陷作图也有广泛认识(见 Knijnenburg,T.A.等,Cell Reports(2018)23:239-254)。 将拓扑异构酶I抑制剂包括SN-38与大分子偶联的报道见下:Zhao ,H .等 , Bioconjugate Chem.(2008)19:849-859和Koizumi,F.等,Cancer Res.(2006)66:10048- 3 CN 111587115 A 说 明 书 2/6 页 10056。本发明中有用的一组特定偶联物公开于Santi ,D .V .等,J .Med .Chem .(2014)57: 2303-2314。还已知另一种偶联物,常称作NKTR-102,是PEG化的伊立替康。 本发明提供了用拓扑异构酶I抑制剂治疗肿瘤对象的改良方法,该方法利用对象 内DDR的固有缺陷(与种系突变或其他对象癌细胞中的功能障碍有关)或与导致合成致死率 的额外药物组合治疗。
技术实现要素:
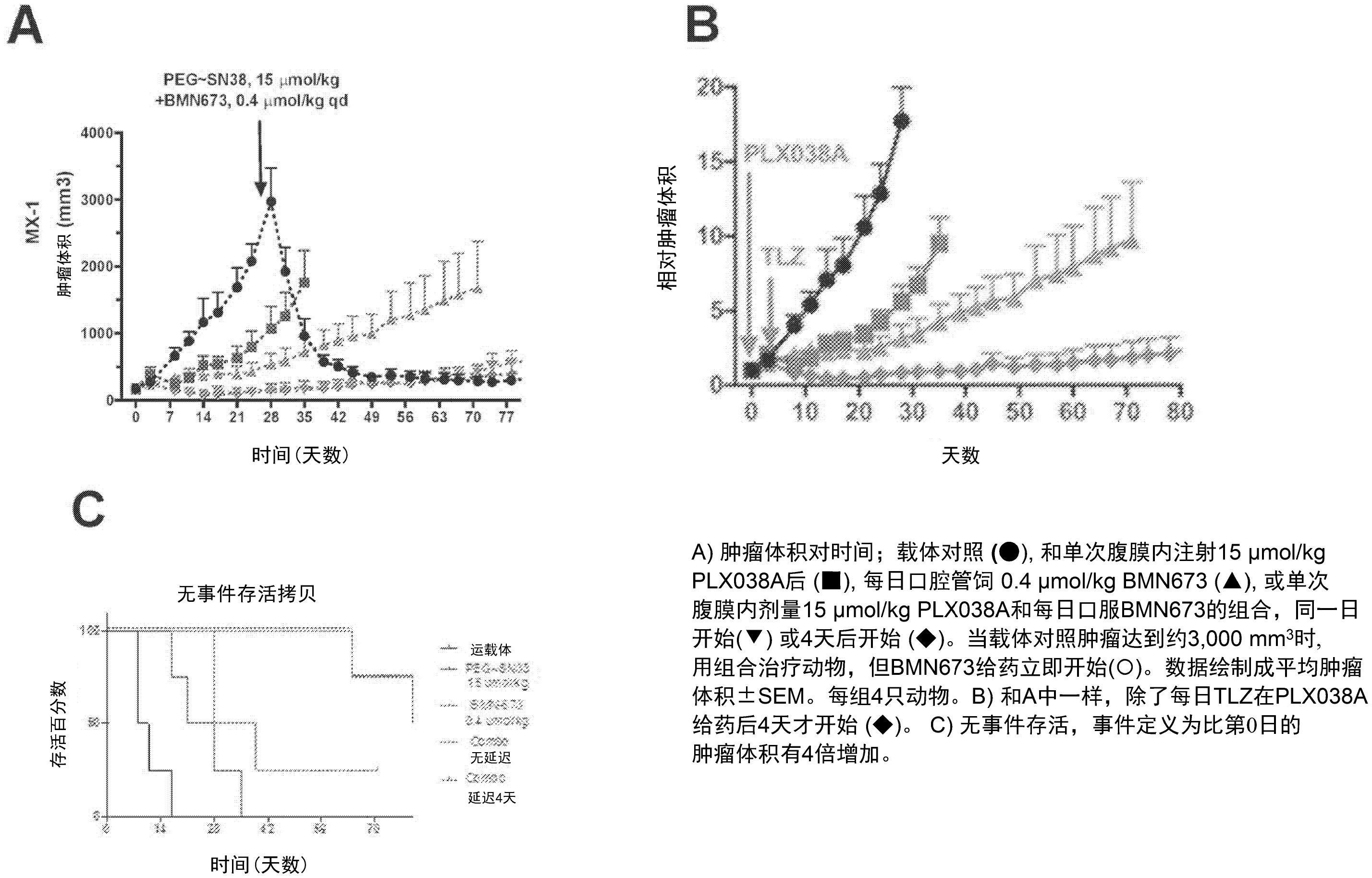
如上述文献所证,已知拓扑异构酶I对于DNA复制是必需的,后者是细胞生长和复 制不可或缺的。拓扑异构酶I抑制剂例如伊立替康及其活性代谢物SN-38已被用于通过抑制 成功DNA复制治疗癌症。 还有报道尝试组合拓扑异构酶I抑制剂和细胞周期检查点抑制剂(中和细胞确定 复制是否成功完成的机制)或额外的DNA损伤反应(DDR)抑制剂。还已知对已经确定具有DDR 缺陷的癌症施用拓扑异构酶I抑制剂。 一些此类尝试涉及与增溶剂例如聚乙二醇(PEG)偶联的拓扑异构酶I抑制剂。然 而,目前提供的该抑制剂的药物动力学并不足以获得成功结果,这些抑制剂的毒性也仍然 有问题。 本发明的方案最重要的是在人类对象中进行,虽然本发明也可用于其他哺乳动物 对象,包括用于测试疾病疗法的实验室模型。方案也可用于牲畜和伴侣动物。 现已发现,提供会通过β消除解偶联的拓扑异构酶I抑制剂连接大分子,或联合细 胞周期检查点通路抑制剂和/或DDR抑制剂,可调节药代动力学,对DDR缺陷对象提供更有效 和更耐受的治疗。本发明的偶联物还可以减少拓扑异构酶I抑制剂和这些额外药剂的协同 毒性的剂量给药。 因此在一个方面,本发明涉及一种在需要治疗的对象中治疗癌症的方法,所述对 象已被鉴定为在DNA损伤反应(DDR)中具有一个或多个缺陷。该方法包括对对象施用有效量 的通过接头偶联于大分子的拓扑异构酶I抑制剂,该接头通过β消除机制提供解偶联。 在第二个方面,本发明涉及一种在对象内治疗癌症的方法,其包括对对象施用有 效量的拓扑异构酶I抑制剂,其通过以β消除提供解偶联的接头与大分子连接,并联合有效 量的额外DDR抑制剂。 在第三个方面,本发明涉及一种在对象内治疗癌症的方法,其包括对对象施用有 效量的拓扑异构酶I抑制剂,其通过以β消除提供解偶联的接头与大分子连接,并联合有效 量的细胞周期检查点通路抑制剂。 在本发明的第一个方面,方法还包括诊断对象中缺陷存在的程序;在施用超过一 种药剂(包括发明偶联物)的实施方式中,超过一种药剂的共同给药可以是同时或以药剂任 意顺序进行。共同给药的药剂施用的时间差异可以长至数日。药剂还可任选的以同一组合 物施用。 上述方法的组合也包括在本发明范围内;因此,可对DDR天然具有缺陷的对象提供 偶联的拓扑异构酶I抑制剂,其通过以β消除机制提供解偶联的接头与大分子偶联,并联合 额外的DDR抑制剂或检查点通路抑制剂或两者。独立地,不论对象是否显示DDR的固有缺陷, 本发明的拓扑异构酶I抑制剂偶联物与额外的DDR抑制剂和细胞周期检查点抑制剂的组合 4 CN 111587115 A 说 明 书 3/6 页 都包括在本发明的范围内。此外,超过一种的DDR抑制剂和/或超过一种的细胞周期检查点 抑制剂与拓扑异构酶I抑制剂偶联物的联合使用也在本发明的范围内。 附图说明 图1显示了本发明方法的示意图,其中栏A中各种修复或细胞周期检查点可能使得 单次用拓扑异构酶I抑制剂处理偏离。当对象具有固有DDR缺陷,例如BRCA基因中的突变,如 栏B所示,拓扑异构酶I抑制的效果被增强,这进一步由DNA损伤修复抑制剂例如PARP抑制剂 增强,例如在栏C中所述(PPAP是聚ADP核糖聚合酶)。 图2显示了各种DDR缺陷对于拓扑异构酶I抑制剂的敏感度的现有技术状态,都涉 及与各种基因相关的非种系DDR中的种系。 图3A-3C显示了本发明的SN-38偶联物和PARP抑制剂对肿瘤生长和无事件存活的 协同效应。 图4A-4C显示了BRCA1或BRCA2缺陷对SN-38偶联物治疗小鼠肿瘤的效力的影响。 本发明的实施方式 本发明利用癌细胞中可能具有的DNA损伤反应的协同攻击以影响其成功复制。导 致DNA损伤的拓扑异构酶I抑制剂偶联物可与DDR抑制剂或其他干涉DNA损伤修复或复制的 抑制剂组合。DDR是极度复杂的过程,涉及各种修复DNA以矫正错误的机制,这些错误通过突 变或通过在复制过程本身中的错误发生。该反应的一部分也是一种控制机制,涉及细胞周 期检查点,其在细胞分裂或产生凋亡前确保DNA正确修复或复制,从而使得携带错误的DNA 不被传递到子细胞中。本发明使用特定DDR抑制剂-拓扑异构酶I抑制剂和其他成功复制障 碍(包括其他DDR抑制剂和细胞周期检查点通路抑制剂)的组合,包括那些癌细胞本身响应 DNA损伤的能力有缺陷的情形。 本发明利用拓扑异构酶I抑制剂与大分子通过接头偶联的偶联物,该接头通过β消 除机制解偶联。合适的拓扑异构酶I抑制剂通常是喜树碱及其类似物,包括伊立替康(也称 作CPT-11)及其活性代谢物SN-38,以及托泊替康、9-氨基-喜树碱及其水溶性类似物例如GI 147211和GI 149893。 在一些实施方式中,大分子是线性或分枝或多臂的聚乙二醇。 特别优选的是式(I)的偶联物 其中, PEG是线性或分枝的,当q是2-8时是多臂的聚乙二醇; 5 CN 111587115 A 说 明 书 4/6 页 X是(CH2)m,其中m=1-6; L是(CH2CH2O)p(CH2)r,其中r=1-10且p=0-10; R1是CN或SO2NR2 ,其中各R22 分别独立地是烷基、芳基、杂芳基、烷基烯基、烷基芳基 或烷基杂芳基,或两个R2合起来能形成环; Y是COR3或SO R32 ,其中R3=OH,烷氧基,或NR4 42,其中各R 分别独立地是烷基,取代的 烷基,或两个R4合起来能形成环;和 q是1-8。 特别是该偶联物可具有平均分子量为30,000-50 ,000Da的PEG,和/或其中q=4, 和/或其中R1=CN或SO2NR22其中各R2是烷基。 偶联物可具有式: 其中m=1-6,n是200-250。 特别是偶联物可以是PLX038,它是上式化合物其中m是1而n是约225。 本发明有用的偶联物一般以标准药物配方联合一种或多种药学可接受的赋形剂 提供,在一些情况下pH是4.0-6.0之间。可在例如Remington Pharmaceutical Sciences,最 新版,Mack Publishing Company,Easton,Pennsylvania中找到标准配方。 本发明基于偶联物的理想性质,该偶联物与内源DDR缺陷或与共同施用的化合物 (细胞周期检查点抑制剂或DDR抑制剂)组合具有合适的药代动力学。 在一些实施方式中,当偶联物施给对象时提供对拓扑异构酶I抑制剂持续的低剂 量接触,其中游离抑制剂的浓度可在每周一次或两次给药之间,或在给药方案期间(例如每 两周一次)维持在15-5nM之间。无论如何,偶联物提供对活性药物持续的低剂量接触。 对于共同给药的DDR抑制剂和/或细胞周期检查点抑制剂,本领域已经有许多了 解,例如上文












