技术摘要:
本发明公开了一种猪胸膜肺炎放线杆菌的LAMP检测试剂盒,具有一检测引物组和一内标引物组;该检测引物组包括一检测外引物对、一检测内引物对和一检测环引物对,该内标引物组包括一内标外引物对、一内标内引物对和一内标环引物对。本发明具有快速高效、操作简便、高特异 全部
背景技术:
胸膜肺炎放线杆菌(Actinobacillus pleuropneumoniae,App)可导致猪传染性胸 膜肺炎,其病理特征是纤维素性胸膜炎和出血性、坏死性脑炎。该病是国际上公认的危害现 代养猪业的五大疾病之一,给各国养猪业造成了巨大的经济损失。此病发病率和致死率极 高,但在大多数病例中呈隐性感染。据报道临床表现健康的猪,其上呼吸道仍有病原体寄 生,这是造成猪胸膜肺炎放线杆菌传播的主要原因,也是造成增重率下降,饲料转化率下 降,上市时间延长的主要原因。尽早诊断亚临床感染病猪是控制该病的关键,但亚临床感染 猪的诊断十分困难。 猪胸膜肺炎放线杆菌现在已发现15个血清型,其中有的不具致病性,有的则会导 致严重疾病。1、5、9、11和12型通常具有很强毒力,而3、6型较为温和。这种细菌寄生于扁桃 体和上呼吸道。病原经飞沫或气雾在短距离内传播,在体外环境只能存活几天。APP对猪致 病有几个毒力因素,包括荚膜多糖、脂多糖、外膜蛋白、转铁结合蛋白、蛋白酶、渗透因子及 溶血素等,在所有致病因子中最重要的是溶血素(Hemolysin,RTX)。APP外毒素 (Actinobacillus pleuropeumoniae-RTX-toxin,Apx)对许多细胞,包括巨嗜细胞具有细胞 毒性作用。在APP的15个血清型中共发现了3种不同的Apx溶血素,即Apx I、Apx II、ApxIII。 前二者具有溶血活性和细胞毒性作用,而ApxIII仅具有细胞毒性作用。1997年Anderso和 Machnnes发现了一个新型Apx毒素,由ApxVII基因编码,它与Apx I、ApxII、ApxIII毒素基因 不同,在所有血清型App中均能检测到。ApxVII基因具有保守性;以App所有15个血清型菌种 做模板,用PCR,方法都能扩增出这条片段,而从其它亲缘关系相近的细菌中无法扩增这一 片段,证明这一片段有很高的种特异性。基于ApxVII的特性,在不分型的情况下,可建立快 速特异的诊断方法,检测出猪胸膜肺炎放线杆菌。所以有学者将胸膜肺炎分子生物学基因 诊断的重点放在ApxVII上。 近年来包括酶联免疫吸附测定(ELISA)、原位杂交、常规PCR、巢式PCR和实时荧光 定量PCR等多种分子生物学检测方法已被开发用于App的诊断检测。其中各种基于PCR的检 测方法具有较高的敏感性和较好的特异性,在实验室检测中应用最为广泛;但是这些方法 需要昂贵的仪器设备、较高检测费用以及对检测人员较高的技术要求,限制了它们在养殖 猪场的实际应用。因此,建立一种可鉴别假阴性检测结果的快速、高通量且对仪器要求不高 的猪胸膜肺炎放线杆菌检测试剂盒及检测方法成为目前急需解决的问题。
技术实现要素:
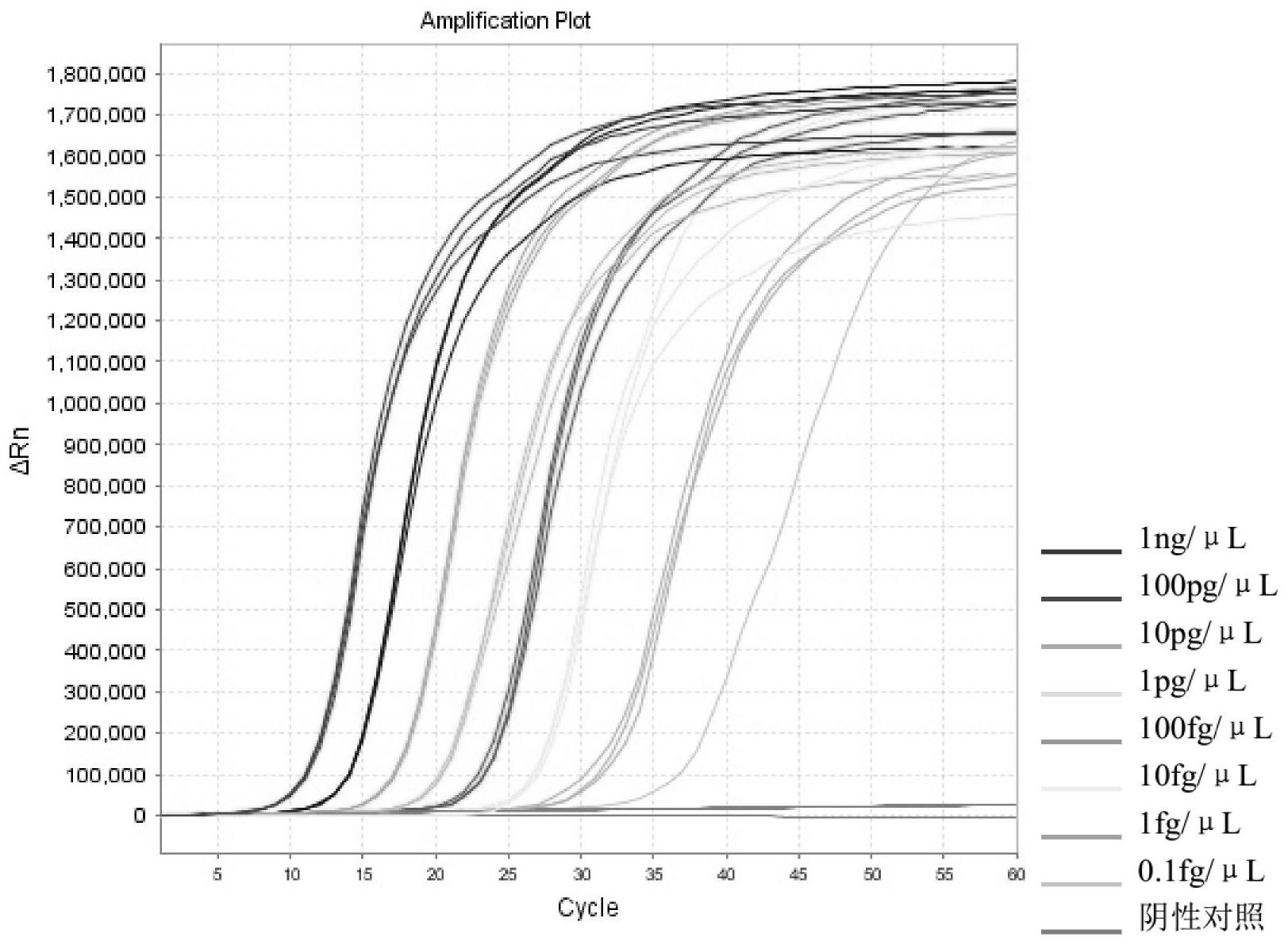
本发明的目的在于克服现有技术缺陷,提供一种猪胸膜肺炎放线杆菌的LAMP检测 试剂盒。 3 CN 111575394 A 说 明 书 2/6 页 本发明的技术方案如下: 一种猪胸膜肺炎放线杆菌的LAMP检测试剂盒,具有一检测引物组和一内标引物 组; 该检测引物组包括一检测外引物对、一检测内引物对和一检测环引物对,该检测 外引物对由如SEQ ID NO.01所示的正向检测外引物和如SEQ ID NO.02所示的反向检测外 引物组成,该检测内引物对由如SEQ ID NO.03所示的正向检测内引物和如SEQ ID NO.04所 示的反向检测内引物组成,该检测环引物对由如SEQ ID NO.05所示的正向检测环引物和如 SEQ ID NO.06所示的反向检测环引物组成; 该内标引物组包括一内标外引物对、一内标内引物对和一内标环引物对,该内标 外引物对由如SEQ ID NO.07所示的正向内标外引物和如SEQ ID NO.08所示的反向内标外 引物组成,该内标内引物对由如SEQ ID NO.09所示的正向内标内引物和如SEQ ID NO.010 所示的反向内标内引物组成,该内标环引物对由如SEQ ID NO.11所示的正向内标环引物和 如SEQ ID NO.12所示的反向内标环引物组成。 在本发明的一个优选实施方案中,所述检测外引物对、检测内引物对和检测环引 物对的摩尔比为1-2∶4-6∶2-4。 在本发明的一个优选实施方案中,所述内标外引物对、内标内引物对和内标环引 物对的摩尔比为1-2∶4-6∶2-4。 在本发明的一个优选实施方案中,还包括DNA聚合酶、LAMP反应液、内标、阳性对照 和阴性对照。 进一步优选的,所述DNA聚合酶为Bst DNA聚合酶。 进一步优选的,所述LAMP反应液中含有浓度为6mM的dNTPs溶液、10×ThermoPol反 应缓冲液和浓度为140mM的MgSO4水溶液。 更进一步优选的,所述dNTPs溶液、10×Thermo Pol反应缓冲液和MgSO4水溶液的 体积比为8∶4∶3。 进一步优选的,所述阳性对照为含有猪胸膜肺炎放线杆菌apxIVA基因片段的T载 体克隆。 进一步优选的,所述阴性对照为超纯水。 进一步优选的,所述内标为含有猪胸膜肺炎放线杆菌omlA基因片段的T载体克隆。 本发明的有益效果是: 1、本发明快速高效:整个扩增只用30-60min即可完成,扩增产量可达109-1010个拷 贝。 2、本发明操作简便:不需要复杂的仪器,不需要特殊试剂,不需要预先进行双链 DNA的变性等繁琐步骤,只需要一部恒定温度仪就能反应和检测,条件比较温和。 3、本发明特异性稿:本发明根据猪胸膜肺炎放线杆菌apxIVA基因设计了检测引物 组,应用这特定的检测引物组,扩增靶序列的6个区域,6个区域中任何区域与引物不匹配均 不能进行核酸扩增,故其特异性极高,且非常稳定,形成引物二聚体概率低,保证了反应的 顺利进行。 4、本发明灵敏度高:最低检测极限可达到1fg/μL。 5、本发明鉴定简便:可通过观察扩增曲线判断扩增与否,无需电泳等其他任何分 4 CN 111575394 A 说 明 书 3/6 页 析步骤,适合现场检测。 6、本发明的准确性高:本发明的检测试剂盒内含内标,可根据检测内标引物组是 否有扩增来判断是否有假阴性检测结果,有效预防因抑制等原因造成的检测结果为假阴性 的情况发生,为目前无法判断检测结果是假阴性结果的情况提供一种新的LAMP检测方法, 提高检测的准确性。 7、本发明的内标与实际样品的检测不在同一管中进行检测,该内标与样品检测管 中的扩增靶标不同,内标的核酸浓度在该内标的检测线附近,可识别轻微的反应抑制;正常 情况下因内标检测管在加入样品提取液的同时加入有低浓度的内标,所以内标检测管检测 检测结果为阳性,如内标管检测结果为阴性,提示样品提取液中含有抑制因子或其他原因, 导致内标检测管不能进行扩增反应,同样样品检测管也可能因抑制因子或其他原因导致不 能进行正常扩增检测,造成样品检测管检测结果为假阴性,因此该方法可根据内标管的检 测结果辅助判断样品检测结果可能为假阴性结果。 附图说明 图1为本发明实施例3的实验结果图之一,其显示猪胸膜肺炎放线杆菌内标的最低 检出限为1fg/μL。 图2为本发明实施例3的实验结果图之二,其为猪胸膜肺炎放线杆菌内标的最低检 出限为1fg/μL的复核。 图3为本发明实施例3的实验结果图之三,其中猪胸膜肺炎放线杆菌apxIVA基因最 低检出限102copies/μL。 图4为本发明实施例4中的特异性实验结果图,其中,对猪链球菌(SS)、猪传染性胃 肠炎病毒(TGEV)、猪瘟病毒(CSFV)、猪蓝耳病毒(PRRSV)、猪圆环病毒2型(PCV-2)、副猪嗜血 杆菌(HPS)、大肠杆菌、金黄色葡萄球菌、猪多杀性巴氏杆菌、健康猪血清临床样本的DNA均 无非特异性扩增。 图5为本发明实施例5的无抑制因子的实际样品检测结果图。 图6为本发明实施例5的有抑制因子的实际样品检测结果图。












