技术摘要:
本发明公开了一种基于量子点胶束球形核酸的DNA机器用于循环miRNA检测的方法。具体实施方法由三部分组成:(1)制备负载DNA酶序列和猝灭剂修饰的底物序列的多色量子点胶束球形核酸(QM‑SNA);(2)在靶标触发且金属离子辅助条件下,DNA酶可实现沿QM表面DNA轨道(底物 全部
背景技术:
microRNA(miRNA)是一类长度约为22个碱基组成的内源性的非编码RNA,可通过抑 制靶向mRNA的表达来调控转录后基因的表达水平,同时miRNA可调控细胞发生、细胞分化、 免疫应答等重要的生理过程,也可作为原癌基因或抑癌基因在不同癌细胞中的异常表达调 控相应的病理过程。多项研究表明,在血液和体液中稳定存在的循环miRNA的异常表达与多 种癌症的发生、发展密切相关,目前已成为一类重要的肿瘤分子标志物。循环miRNA具有序 列短、相似度高、丰度较低,且一条miRNA可作用于多条mRNA,多条miRNA又可以同时作用于 一条mRNA分子的特性。因此,如何开发出一种具有高灵敏、高特异性、多元检测能力的循环 miRNA检测方法成为现阶段的巨大挑战。 传统的miRNA检测方法包括PCR法、微阵列法、测序法。PCR法检测miRNA具有较高的 灵敏度和准确度,但检测过程包括引物设计、温度调控等相对复杂。微阵列和测序方法具有 高通量检测的优势,但通常不兼容扩增过程,因而在灵敏度和特异性方面还有待改善,并且 成本相对较高。荧光传感器具有制备简单和检测灵敏度高等优点,目前已成为miRNA检测的 研究热点。量子点作为一种新型荧光团,具有抗光漂白性好、亮度高、单一波长激发多色发 射等优良的光学性质,通过表面功能化可方便制备荧光传感器。现有的量子点荧光传感器 大多是通过配体交换方法赋予其良好的水溶性,但制备时间较长,且荧光量子产率发生较 大程度的下降。更为重要的是,配体交换方法制备的水溶性量子点粒径小,不便于功能性核 酸的进一步集成。与之相对比,量子点胶束(QM)方法即直接在油溶量子点表面通过疏水作 用包覆磷脂制成胶束的方法,具有制备简单的优势,并且保持了内核油溶性量子点高的荧 光量子产率。同时量子点胶束有效增大了表面积,便于进一步的功能化如功能性核酸的集 成等,因而更便于其在生物传感领域的应用。 miRNA低丰度的特点要求对miRNA的检测通常需要信号放大技术的辅助。目前发展 的多种等温扩增技术如链式杂交反应(HCR)、滚环扩增反应(RCA)、链式取代反应(SDA)、催 化发卡自组装(CHA)和DNA纳米机器(如DNA酶步行器)等均可实现有效的信号放大。DNA酶步 行器是在无蛋白酶参与下利用金属离子DNA酶自身具有的催化活性对底物进行剪切并沿特 定的轨道实现自动化行走。相比于蛋白酶,金属离子DNA酶具有合成成本低、结构稳定的显 著优势。金属离子DNA酶行走具有条件温和、自动化、高效等优点,为检测miRNA提供了新的 方法。
技术实现要素:
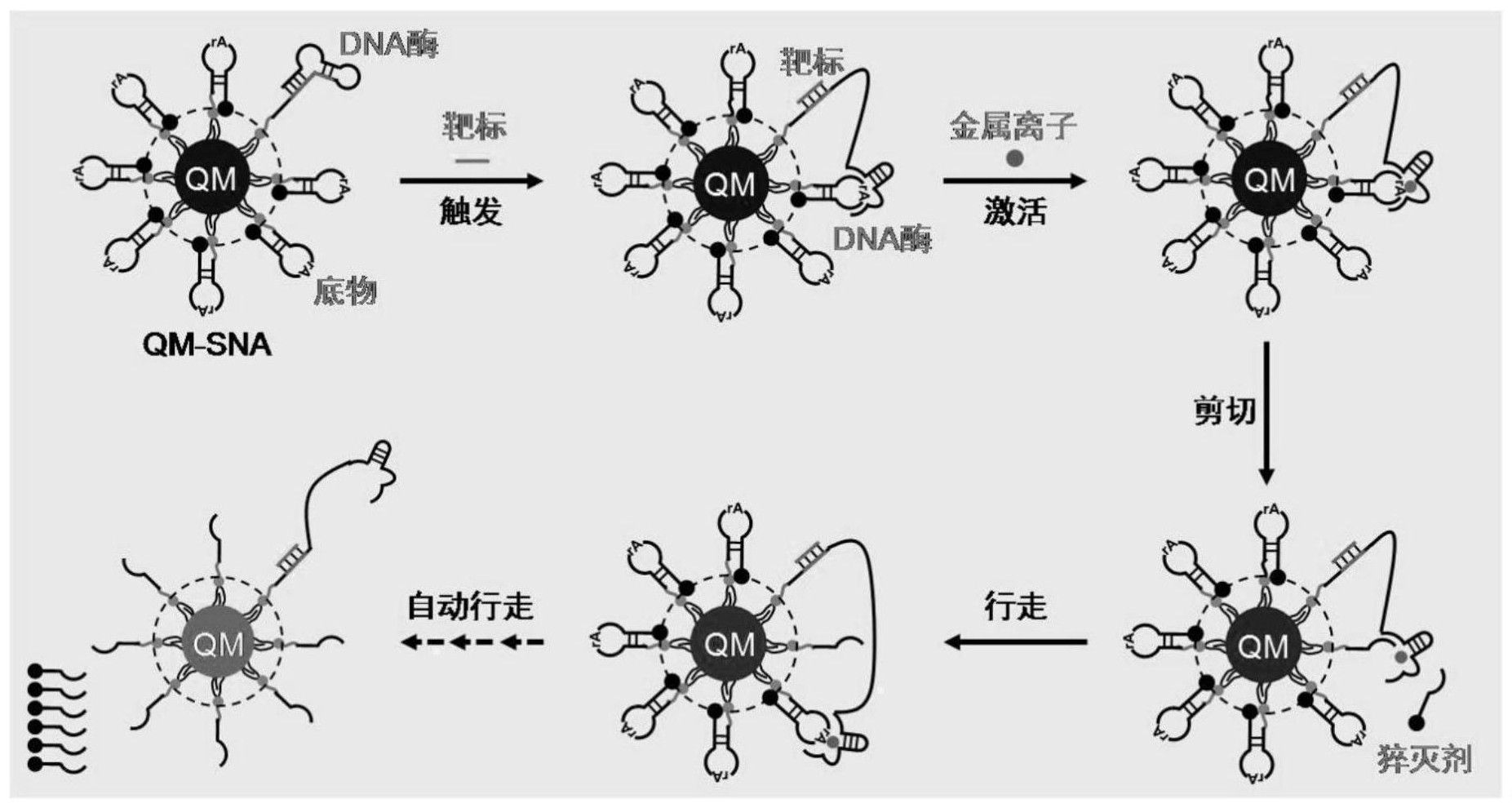
技术问题:针对上述问题,本发明提供了一种基于量子点胶束球形核酸(QM-SNA) 3 CN 111593094 A 说 明 书 2/6 页 的DNA机器用于循环miRNA的检测方法,可以实现对循环miRNA的高灵敏度和多元检测。 技术方案:为了实现上述目的,本发明采用了以下技术方案,具体步骤包括: (1)制备负载DNA酶和猝灭剂修饰的底物的多色量子点胶束球形核酸(QM-SNA); (2)靶标miRNA触发金属离子DNA酶沿QM(量子点胶束)表面DNA轨道(底物序列)的 自动化行走; (3)采用荧光分光光度计测量步骤(2)中行走结束后QM的荧光信号,对循环miRNA 进行多元检测分析。 其中,步骤(1)中所述的负载DNA酶及其底物的QM-SNA,包括三种量子点胶束(QM)、 三种靶标、三种DNA酶序列及其底物序列和金属离子。三种QM分别由绿、黄、红三种颜色的量 子点制备而成;三种靶标分子为血清中的三种循环miRNA,如非小细胞肺癌标志物miRNA- 196a、miRNA-25、miRNA-21;三种DNA酶和对应的底物均为茎环结构,其序列分别为DNAzyme 1/Substrate 1、DNAzyme 2/Substrate 2、DNAzyme 3/Substrate 3,DNAzyme的5’端修饰氨 基,Substrate的5’端和3’端分别修饰猝灭剂(BHQ)和氨基。其中DNAzyme 1/Substrate 1用 于检测miRNA 1,偶联至绿色的QM表面;DNAzyme 2/Substrate 2用于检测miRNA 2,偶联至 黄色的QM表面;DNAzyme 3/Substrate 3用于检测miRNA3,偶联至红色的QM表面。由于偶联 猝灭剂修饰的底物,三种QM的荧光均处于猝灭状态。采用的金属离子为锌离子或镁离子。 步骤(2)中所述的靶标miRNA触发并在金属离子辅助条件下,DNA酶沿QM表面DNA轨 道的行走。靶标不存在的条件下,DNA酶上下臂封闭。加入miRNA,靶标与DNA酶杂交打开DNA 酶的封闭区域,释放出上下臂,上下臂与相邻底物杂交并结合金属离子,激活DNA酶的催化 中心,剪切底物上的rA位点,释放5’端猝灭剂(BHQ)修饰的底物片段。由于DNA酶的下臂与剩 余底物片段之间结合力较弱,DNA酶的上下臂重新释放出来,并行走至下一个底物与之杂 交、剪切。经过DNA酶执行多次“识别-剪切-释放”的行走过程后,最终能剪切掉QM表面所有 的底物序列。由于大量的BHQ脱离QM表面,QM荧光信号最大程度恢复。 步骤(3)中所述的采用荧光分光光度计测量步骤(2)中DNA酶行走结束后多色QM的 荧光信号,实现miRNA的多元检测分析。三色QM荧光发射波长标记三种靶标miRNA,QM荧光强 度标定靶标miRNA数量。QM荧光强度与靶标丰度之间存在线性关系,绘制标准曲线。通过测 量实际样品中多色QM的荧光光谱,可实现靶标定量。 有益效果:与现有的技术相比,本发明制备了负载DNA酶步行器的多色量子点胶束 球形核酸(QM-SNA)荧光传感器,通过靶标触发DNA酶自动行走介导的QM荧光增强,实现对循 环miRNA的高灵敏度和多元检测。 检测(行走)时间:40分钟;检测限:10飞摩(fM);可同时检测至少三种靶标miRNA。 附图说明 图1为基于QM-SNA的DNA酶行走过程示意图; 图2为QM与QM-SNA的性质表征; 图3为QM表面DNA酶行走的时间动力学; 图4为DNA酶步行器检测miRNAs的灵敏度和标准曲线; 图5为DNA酶步行器检测miRNAs的特异性; 图6为DNA酶步行器检测miRNAs的多元能力评估; 4 CN 111593094 A 说 明 书 3/6 页 图7为DNA酶步行器多元检测血清中循环miRNAs。












