技术摘要:
本发明提供一种去除大肠杆菌表达重组猪细小病毒VP2蛋白中内毒素的方法,包括猪细小病毒重组VP2蛋白抗原溶液制备、氢氧化铝悬液制备、氢氧化铝吸附和层析法分离步骤。通过氢氧化铝吸附和复合模式层析介质分离两步,可以有效去除大肠杆菌表达系统中重组蛋白的内毒素,操 全部
背景技术:
内毒素(endotoxin)是存在于革兰氏阴性菌细胞壁外膜表面的一种大分子物质, 一般在细胞死亡或分解时自行释放到周围介质中,也可以从活细胞中直接泄漏出来。因为 革兰氏阴性菌无处不在,所以内毒素几乎存在于任何地方。在疫苗生产中一定要重视和尽 可能减少内毒素的污染。生产用水中内毒素的含量是导致疫苗安全性的关键因素之一。大 量研究表明,疫苗生产过程中内毒素主要来源于培养液和配制用水,其在贮存过程中易受 到革兰氏阴性菌的污染。生产用具、管道、泵、阀门、滤器等的清洗消毒不彻底也会造成内毒 素污染。生产原料的污染,如血液制品,细胞培养基。人为操作不规范也会引起内毒素污染。 而生物制品中,内毒素的污染广泛存在,比如,单克隆抗体作为生物大分子药物,生产和纯 化工艺复杂,有诸多环节可能将内毒素带入,因此需要去除内毒素,保证生物制品的安全 性。各国药监部门对生物产品中的内毒素含量也均有严格规定。欧洲药典规定注射剂内毒 素限度不得高于5EU/(kg·h),EU为内毒素单位,每EU内毒素约相当于100pg。随着生物制品 的大量使用,对生物制品中内毒素残留限的要求越高,但是因为内毒素分子结构复杂且不 均一,导致内毒素可以多种方式与溶液中的蛋白质相互作用,形成复合物,大大增加了去除 的难度。并且,在去除内毒素的同时,还要尽可能减小活性成分的损失。 猪细小病毒(porcine parvovirus,PPV)是一种DNA病毒,主要引起猪细小病毒病, 又称为猪繁殖障碍病。该病以怀孕母猪发生流产、死胎、产木乃伊为特征,特别是初产母猪 发病率较高,但母猪本身无明显的症状。因此,该病难以察觉,危害极大,严重影响母猪的生 产繁育。VP2蛋白是PPV的主要结构蛋白,重组VP2蛋白免疫原性强,能够刺激强的免疫应答 反应,是理想的PPV疫苗靶标。大肠杆菌重组表达PPVVP2蛋白具有良好的蛋白结构和免疫原 性,产量高生产成本低,操作简单,是生产猪细小病毒疫苗的理想抗原。但是大肠杆菌含有 大量的内毒素,重组大肠杆菌细胞经破碎后内毒素释放到蛋白溶液中,其含量可以达到 106EU以上。由于内毒素含量高,采用传统方法清除较为困难,严重影响了大肠杆菌重组表 达PPVVP2蛋白在生物制品领域的应用。目前,常用的去除内毒素的方法有活性炭吸附、萃 取、超滤、离子交换色谱等,不同的技术方案适合不同的应用场景,但是这些方案总体存在 内毒去除效果不佳、清除效率太低、成本过高等问题,是生产中的一大难题。经检索,发明专 利申请《一种生物制品的内毒素去除方法》(CN 104710527A)提出一种利用羟基磷灰石去除 内毒素的技术方法,由于该方法所用基质羟基磷灰石的内毒素载量有限,因此内毒素去除 效率较低,适合用于动物细胞表达系统表达生物制品或者单克隆抗体等内毒素含量较低 (100EU/mg以下)的样品中内毒素的去除。若用于大肠杆菌中内毒素清除需要消耗大量羟基 磷灰石,成本昂贵,处理能力有限,不适合用于清除大肠杆菌来源的生物制品中的106EU以 4 CN 111606978 A 说 明 书 2/7 页 上内毒素的清除。
技术实现要素:
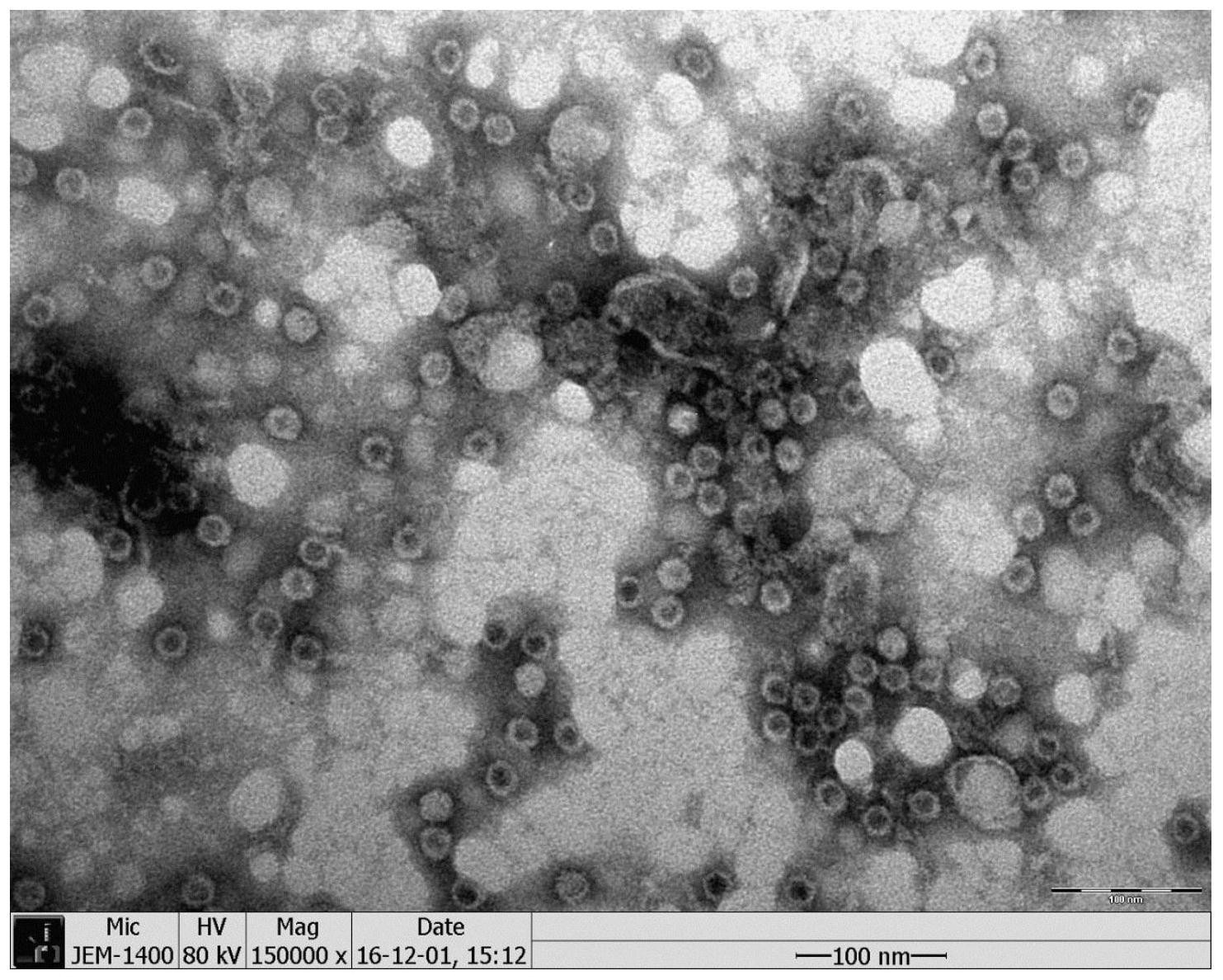
针对现有技术的不足,本发明的目的是提供一种去除大肠杆菌表达重组猪细小病 毒VP2蛋白中内毒素的方法,该方法针对大肠杆菌表达重组猪细小病毒VP2蛋白的理化特性 和内毒素特征,提出一种包括氢氧化铝吸附和复合模式层析介质分离的两步法,用于清除 重组PPV VP2蛋白中的内毒素,解决PPV疫苗生产中的核心技术问题。 为了实现上述目的,本发明所采用的技术方案是: 一种去除大肠杆菌重组表达猪细小病毒VP2蛋白中内毒素的方法,包括如下步骤: (1)猪细小病毒重组VP2蛋白抗原溶液的制备:采用大肠杆菌表达系统重组表达猪 细小病毒VP2蛋白,经高速离心、硫酸铵沉淀,收集得猪细小病毒重组VP2蛋白抗原溶液; (2)氢氧化铝悬液的制备:将氢氧化钠和氯化铝混合,pH为6.0~6.8,在2~8℃条 件下反应,得到20g/L的氢氧化铝悬液; (3)氢氧化铝吸附:对步骤(1)所得的猪细小病毒重组VP2蛋白抗原溶液进行预处 理,随后缓慢加入步骤(2)所得的氢氧化铝悬液进行吸附,边加入边搅拌,温度为2~8℃,转 速为100rpm,搅拌时间为1~3h,搅拌完成后,离心处理得去除内毒素后的蛋白溶液上清液; 重复氢氧化铝悬液吸附1次;其中每次氢氧化铝悬液的加入量均按Al2O3的浓度计 算,当Al2O3在VP2蛋白抗原溶液中的浓度为0.1mg/mL时,停止加入氢氧化铝悬液; (4)层析法分离:采用吸附层析法,将步骤(3)所得的去除内毒素后的蛋白溶液上 清液进行预处理,随后以一定的流速上样到层析介质,上样前先用清洗液清洗层析柱,然后 用平衡缓冲液平衡层析柱,上样时收集上样流穿溶液,上样完成后用2倍柱体积的平衡缓冲 液冲洗层析柱,收集层析柱流出液,合并流穿溶液与层析柱流出液,得到去除内毒素的猪细 小病毒重组VP2蛋白抗原溶液。 所述步骤(1)中大肠杆菌表达系统重组表达猪细小病毒VP2蛋白的方法为:构建猪 细小病毒VP2蛋白重组表达菌株,将活化后的猪细小病毒VP2重组菌株接种于LB培养基,在 温度37℃、转速220rpm摇床培养3~5h,待菌株培养液的吸光值OD600达到0.8~1.2,加入终 浓度为0.1~0.15mM IPTG诱导重组表达的猪细小病毒VP2蛋白,在温度25℃、转速220rpm摇 床中继续培养12~16h。 所述步骤(1)中猪细小病毒VP2蛋白抗原溶液的收集方法具体为: a、以8000rpm的转速离心处理经大肠杆菌表达系统重组表达的猪细小病毒VP2蛋 白溶液,收集离心后沉淀,即得到重组表达VP2蛋白大肠杆菌菌体,称量菌体湿重,加入pH值 为6.3的10mM PB缓冲液重悬菌体,其中菌体湿重的质量与PB缓冲液的体积比为1:20; b、将步骤a经PB缓冲液重悬后的大肠杆菌菌体,先用超声破碎或高压均质机破碎, 再以8000rpm的转速离心处理破碎的菌体,收集离心后上清,去除破碎菌体碎片,即得到破 碎菌体上清溶液; c、向步骤b收集的破碎菌体上清溶液中加入硫酸铵,边加入边搅拌,形成40%饱和 度的硫酸铵溶液,以100rpm的转速持续搅拌2h后,再以8000rpm的转速,2~8℃条件下离心 30min,收集离心后沉淀; d、向步骤c收集的沉淀中加入10mM PBS缓冲液使沉淀溶解,加入的PBS缓冲液体积 5 CN 111606978 A 说 明 书 3/7 页 与步骤(a)中的PB缓冲液的体积相同,即得猪细小病毒重组VP2蛋白抗原溶液。 其中超声破碎的条件为:工作3s、间歇5s、功率60w、时间15min,将重悬的菌液置于 冰水混合浴中,探头插入液面以下1.0~2.0cm,开始超声破碎; 高压均质机破碎的条件为:压力800bar,温度控制在5~10℃,进样速度为480mL/ min,高压破碎1遍。 所述步骤(3)中猪细小病毒重组VP2蛋白抗原溶液预处理的方法为:加入10mM PB 缓冲液,调整pH为6.0~6.8,温度为2~8℃;所述离心处理的离心力为7000g~9000g,离心 温度为4-8℃,离心时间为20~40min。 所述步骤(3)中猪细小病毒重组VP2蛋白抗原溶液预处理的方法为:加入10mM PB 缓冲液,调整pH为6.2~6.5,温度为2~8℃;所述离心处理的离心力为8000g,离心温度为6 ℃,离心时间为30min。 所述步骤(4)中去除内毒素后的蛋白溶液上清液预处理的方法为:加入含200mM氯 化钠的10mM PB缓冲液,调整pH为8.0,在2~8℃下搅拌3~5h。 所述步骤(2)中的pH为6.2~6.5;所述步骤(3)中的搅拌时间为2小时。 所述步骤(4)中吸附层析法所用填料为复合模式层析介质CaptoTMCore700;所用清 洗液为含有30%(体积含量)异丙醇的1mol/LNaOH;所用平衡缓冲液pH为8.0、含200mM氯化 钠的10mM PB缓冲液;流速为1/10~1/20柱体积每分钟。 所述去除内毒素的猪细小病毒重组VP2蛋白在制备疫苗和药物制剂类生物制品中 的应用。 本发明有益效果: 1、本发明利用氢氧化铝凝胶带正电荷的特性,在pH为6.2~6.5的条件下,可与内 毒素中带负电的磷酸基团共价结合,而PB缓冲液中磷酸根和合适的pH条件,可降低或防止 氢氧化铝对VP2蛋白抗原的吸附,降低VP2蛋白的损失,从而有效吸附溶液的内毒素。 2、本发明利用VP2蛋白在体外可自动组装形成病毒样颗粒(virus-like particles,VLPs)的特性,将氢氧化铝处理后的VP2蛋白溶液在2~8℃,pH为8.0,含有200mM NaCl的10mM PB缓冲液中搅拌4h以上,促进重组VP2蛋白组装成VLPs,组装效率可达90%以 上,其粒径在20-30nm之间,具备红细胞凝集活性。 3、本发明利用复合模式层析介质CaptoTMCore700具有分离以及吸附层析的双重功 能,VP2蛋白形成的病毒样颗粒在层析柱的穿流中被收集起来,同时较小的杂质以及内毒素 会与微球内在配基结合,达到对VP2蛋白溶液中内毒素进一步净化的目的。与传统凝集过滤 层析、离子交换层析相比,本发明中采用的层析介质具备高载量、高流速和操作简单方便等 特点,显著提高生产效率,适合生物制品大规模生产使用。 4、本发明提供的氢氧化铝吸附和复合模式层析介质CaptoTMCore700分离两步法, 可以有效去除大肠杆菌表达系统中重组蛋白的内毒素,方法操作简单实用,符合规模化生 产的需求。采用本发明方法处理后的生物制品的VP2蛋白内毒素含量小于200EU/mL,且对 VP2蛋白的抗原活性无明显影响,安全性好,具有良好的临床应用前景。 5、控制药品中内毒素含量,对疫苗和蛋白质药物的研究至关重要,含内毒素制剂 注射到人和动物体内会引起发热、休克、多器官损伤甚至死亡。大肠杆菌表达系统具有产量 高、成本低、操作简便等优点,但是该内毒素含量限制了该技术在疫苗和制药领域的应用, 6 CN 111606978 A 说 明 书 4/7 页 本申请提供一种高效、便捷的去除大肠杆菌重组表达PPVVP2蛋白内毒素的方法,处理后的 蛋白可在制备疫苗、药物类等生物制品中应用,解决了PPV疫苗生产中的核心技术问题。 附图说明 图1猪细小病毒VP2蛋白病毒样颗粒电镜图; 图2猪细小病毒VP2蛋白病毒样颗粒动态光散射图。












