技术摘要:
本发明公开一种SUMO化修饰的多肽或小分子蛋白靶向释药载体,由能够被SUMO化修饰的小分子蛋白或多肽及SUMO化修饰结构构成,能够被SUMO化修饰的小分子蛋白或多肽和药物分子偶联,小分子蛋白或多肽再进一步SUMO化修饰后构成靶向药物,可以实现肿瘤组织细胞内定位和分布, 全部
背景技术:
在新型药物传输系统研究中,提高药物对肿瘤治疗的选择性,已成为抗肿瘤药物 研究的一个活跃课题。近年来,肿瘤的药物靶向治疗研究取得了很大进展。用载体将抗癌药 运送到肿瘤组织(靶区),使之形成一个高于正常组织的药物浓度,并延缓药物在肿瘤组织 中的释放,大大地提高了药物的疗效,减低了毒副作用。 国内外对药物载体及药物缓释制剂开展了广泛的研究。常见的药物载体有O/W乳 状液、聚合物粒子、脂质体或纳米粒子等。然而,将O/W乳状液作为药物载体存在不稳定的问 题;聚合物粒子虽然由于粒子小可穿越生物膜屏障到达人体的特定部位,但毒副作用大;脂 质体作为药物载体有较好的生物相容性和靶向性,但热力学不稳定,粒径较大,易被单核吞 噬细胞系统所吸收;纳米粒子(NP)可采用特殊材料或表面修饰达到靶向目的,有利于难溶 性药物的吸收和提高药物的生物利用度,稳定性好,也是目前国内外实现肿瘤靶向治疗的 研究热点,但是其主要还是依赖网状内皮细胞吞噬、机械性滤阻来实现靶向给药目的,特异 性并不高,而且存在潜在的聚积风险。 多肽和小分子蛋白分子结构简单、种类繁多、易于改进、性质相对稳定,是靶向药 物载体的理想构造单元,多肽和小分子蛋白作为药物、基因的载体材料,因其特殊的结构、 生物相容性以及靶向穿透性,而备受研究者的关注。多肽或小分子蛋白作为靶向药物载体 具有转运效率高、毒性低,对所载物质的大小无限制,不引起炎症反应等优点,但是多肽或 小分子蛋白类载体本身是蛋白酶的底物,在组织细胞内很容易经蛋白酶体途径降解,从而 局限了其在药物转运领域的应用。
技术实现要素:
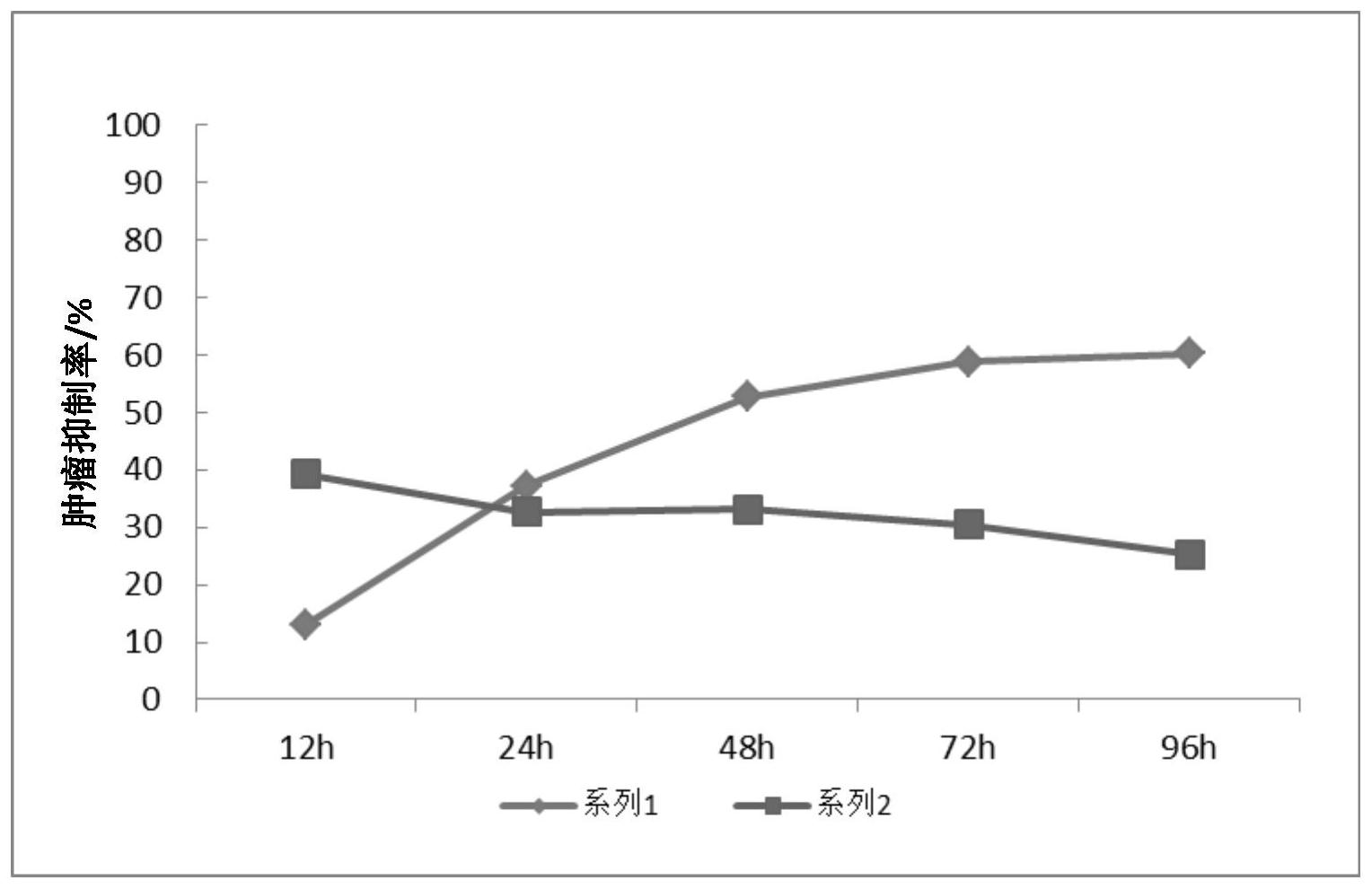
本发明的目的是提供一种SUMO化修饰的多肽或小分子蛋白靶向释药载体,以解决 现有技术的不足。 本发明采用以下技术方案: 一种SUMO化修饰的多肽或小分子蛋白靶向释药载体,由能够被SUMO化修饰的小分 子蛋白或多肽及SUMO化修饰结构构成, 能够被SUMO化修饰的小分子蛋白或多肽和药物分子偶联,小分子蛋白或多肽再进 一步SUMO化修饰后构成靶向药物,实现肿瘤组织细胞内定位和分布,并且避免在细胞内过 早被组织蛋白酶降解,最终在肿瘤组织高效表达的SENP1作用下解离SUMO亚基,去SUMO化的 小分子蛋白或多肽很快被组织蛋白酶降解,而完成释药。 进一步地,能够被SUMO化修饰的小分子蛋白或多肽包括RanGAP1、RanBP2、HIPK2、 Daxx、CaMK、SF-1、AIRE、CREB、SP100、IkBα、HIF1α、P53、C-Jun小分子蛋白或其部分序列。 3 CN 111588863 A 说 明 书 2/4 页 进一步地,能够被SUMO化修饰的小分子蛋白或多肽和药物分子共价偶联。 进一步地,能够被SUMO化修饰的小分子蛋白或多肽的氨基酸残基和药物分子通过 共价偶联形成酯键/酰胺键。 进一步地,在适宜的反应体系中,由激活酶E1、接合酶E2或激活酶E1、接合酶E2、连 接酶E3把SUMO蛋白转移到所选小分子蛋白或多肽底物上,最终将SUMO通过异肽键偶联到小 分子蛋白或多肽底物的赖氨酸残基上,完成SUMO化修饰。 进一步地,SUMO蛋白包括SUMO-1、SUMO-2、SUMO-3、SUMO-4。 本发明的有益效果: 1 .肿瘤缺氧条件下的增殖,有赖于HIF1α对血管内皮生长因子(VEGF)的调控,而 HIF1α稳定与活性,依赖SENP1在缺氧条件下的高表达。肿瘤组织中高浓度的SENP1,可以高 效进行SUMO化修饰的多肽或小分子蛋白靶向释药载体的去SUMO化,从而实现药物在肿瘤组 织中的靶向释放。 2.SUMO化修饰决定了底物多肽或小分子蛋白靶向释药载体在肿瘤组织细胞内的 定位、分布和稳定性,并在协同蛋白泛素化降解等方面发挥着重要作用,赋予药物靶向性和 稳定性特征。 3.利用人体肿瘤组织内高效表达的蛋白酶SENP1,实现去SUMO化,多肽或小分子蛋 白经蛋白酶体途径降解,实现多肽或小分子蛋白靶向释药载体定向释药,靶向性高、释药平 稳。 附图说明 图1为实施例2SDS-PAGE电泳图。 图2为实施例3药物释放过程(系列1:SUMO1Ran GAP1-C2Fu-O-G在正常肝细胞中的 释放过程,系列2:SUMO1…Ran GAP1-C2…Fu-O-G在癌细胞SMMC7721中的释放过程,系列3: Ran GAP1-C2…Fu-O-G在正常肝细胞中的释放过程,系列4:Ran GAP1-C2…Fu-O-G在癌细胞 SMMC7721中的释放过程)。 图3为实施例3药物肿瘤抑制结果(系列1:SUMO1Ran GAP1-C2Fu-O-G对癌细胞 SMMC7721的抑制,系列2:Ran GAP1-C2…Fu-O-G对癌细胞SMMC7721的抑制)。












