技术摘要:
本发明分离的T细胞受体和应用,所述分离的T细胞受体包括α链和β链中的至少一者,β链可变区的CDR3具有SEQ ID NO.7至10任一所示的序列,用此TCR修饰的免疫细胞具有显著的抗肿瘤效果。
背景技术:
T细胞相关免疫疗法在近期的癌症研究中大放异彩,“主力部队”是CAR-T和TCR-T 这两种技术。相对于CAR-T细胞疗法,TCR-T疗法的关注度相对低些,但是这两种细胞疗法都 属于利用患者自身的T淋巴细胞治疗癌症的前沿基因疗法。TCR-T疗法通过转导嵌合抗原受 体或者TCRα/β异二聚体,来提高特异性识别肿瘤相关抗原(Tumor Associated Antigen , TAA)的TCR(T cell receptor,T细胞抗原受体)的亲和力和战斗力,使T淋巴细胞能够重新 高效的识别靶细胞。通过输注能够识别特异靶标的基因修饰T淋巴细胞,TCR-T疗法赋予免 疫系统以新的非自然免疫活性。这种方法除了能像化疗和靶向治疗一样快速杀灭肿瘤外, 还避免了疫苗和T淋巴细胞检查点疗法的延迟效应。 目前已知,TCR的多肽链依据抗原结构和编码基因的不同,有α、β、γ和δ4种。TCR分 子的4条多肽链可分为细胞外、跨膜和细胞质3部分,其中肽链氨基端在细胞外,羧基端在细 胞内;氨基端肽链的氨基酸顺序变化较大,称为可变域;近膜端肽链的氨基酸顺序变化少, 称为保守域。根据受控基因片段的不同,细胞外肽链又分为V(可变区)、D(高变区)、J(结合 区)和C(恒定区)4个区域,其中α链由V、J和C基因节段编码,β链由V、D、J和C基因节段编码。 细胞外肽链的可变域存在4个互补结合功能区(complementary determining religion, CDR)。V基因编码CDR1和CDR2,而CDR3是唯一非胚系编码的抗原特异性结合部位。TCR基因多 态性主要由CDR3决定。 到目前为止,TCR-T细胞免疫疗法已在部分实体肿瘤的治疗中取得了较好的疗效, 但是仍存在受抗原限制、杀伤活性低等缺点,研究高效、低毒及可操控的TCR-T细胞免疫法 在肿瘤治疗中具有理想的应用前景。
技术实现要素:
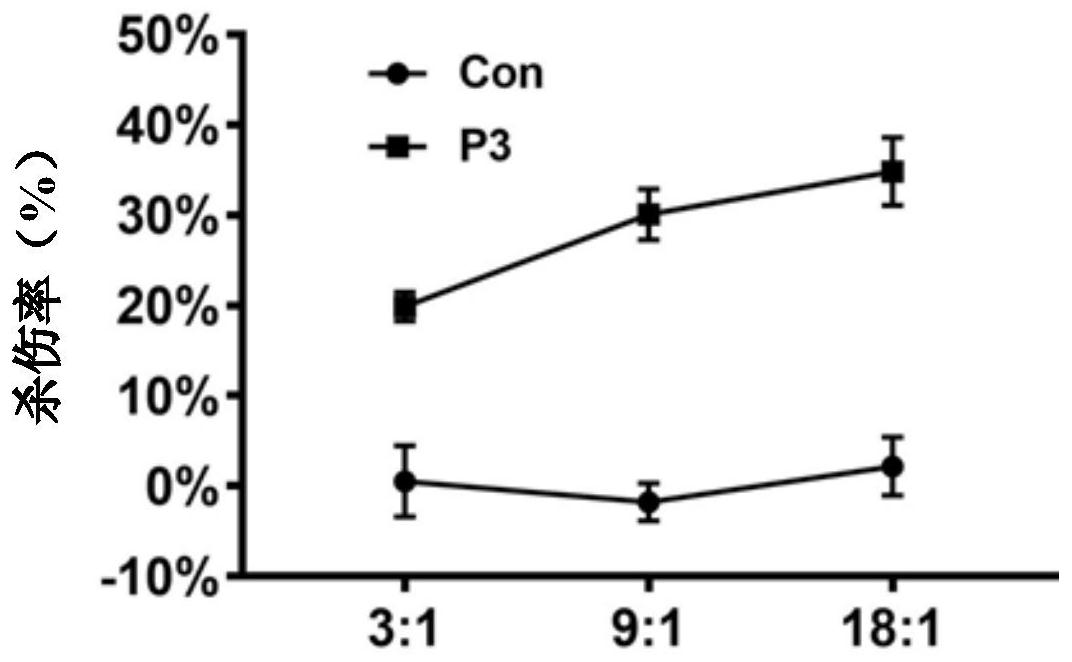
为了弥补现有技术的不足,本发明提供一种的分离的T细胞受体以及与该受体相 关的核酸、重组表达载体、T细胞。本发明还提供了用于治疗或预防肿瘤和/或癌症、或用于 检测宿主的肿瘤和/或癌症的包含T细胞受体的药物组合物。本发明提供的T细胞受体及其 相关的产品具有较好的杀伤效果。 具体而言,本发明提供了如下内容: (1)一种分离的T细胞受体,包所述括α链和β链中的至少一者,β链可变区的CDR3具 有SEQ ID NO.7至10任一所示的序列。 根据(1)所述的T细胞受体,所述T细胞受体的β链可变区的CDR1序列和CDR2序列分 别具有如SEQ ID NO.5和6所示的序列。 作为一种优选的实施方式,所述T细胞受体的β链可变区具有SEQ ID NO.11所示的 3 CN 111574616 A 说 明 书 2/9 页 氨基酸序列。 作为另外一种优选的实施方式,所述T细胞受体的β链可变区具有SEQ ID NO.12所 示的氨基酸序列。 作为作为另外一种优选的实施方式,所述T细胞受体的β链可变区具有SEQ ID NO.13所示的氨基酸序列。 作为作为另外一种优选的实施方式,所述T细胞受体的β链可变区具有SEQ ID NO.14所示的氨基酸序列。 根据(1)所述的T细胞受体,所述T细胞受体的α链可变区的CDR3具有SEQ ID NO.3 所示的序列。 作为一种优选的实施方式,α链可变区的CDR1和CDR2具有SEQ ID NO .1和SEQ ID NO.2所示的序列。 (2)一种分离的分离的、编码T细胞受体的核酸,所述核酸编码(1)所述的T细胞受 体,或α或β链,或可变结构域,或具有结合抗原能力的片段。 作为一种优选的实施方式,本发明的核酸的核苷酸序列进行编码子优化以增加基 因表达、蛋白翻译效率以及蛋白表达,从而增强TCR识别抗原的能力。编码子优化包括但不 限于翻译启动区域的修饰、改变mRNA结构片段、以及使用编码同一氨基酸的不同密码子。 在其它的实施方案中,可以对上述TCR编码核酸的序列进行突变,包括去除、插入 和/或置换一个或多个氨基酸密码子,使得所表达的TCR识别抗原的功能不变或者增强。例 如,在一个实施方案中,进行保守氨基酸置换,包括对上述TCRα链和/或β链的可变区中的一 个氨基酸用结构和/或化学属性相似的另一个氨基酸进行置换。术语“相似的氨基酸”是指 具有相似的极性、电负荷、可溶性、疏水性、亲水性等属性的氨基酸残基。突变后的TCR仍具 有识别上述被靶细胞提呈的抗原多肽的生物活性。 (3)一种重组表达载体,含有与启动子有效连接的、(2)中所述的核酸,和/或其互 补序列。 作为一种优选的实施方式,在所述重组表达载体中,本发明所述的DNA合适地与启 动子、增强子、终止子和/或polyA信号序列有效连接。本发明的重组表达载体的上述作用元 件的组合能够促进DNA的转录和翻译,并增强mRNA的稳定性。 在一个实施方案中,重组表达载体上的α链和β链基因的表达可以由两个不同的启 动子所驱动,启动子包括各种已知的类型,例如强表达的、弱表达的、可诱导的、组织特异性 的、和分化特异性的启动子。启动子可以是病毒来源的或者非病毒来源的,例如CMV启动子、 MSCV的LTR上的启动子、EF1-α启动子、和PGK-1启动子。两个启动子的驱动方向可以是同向 也可以是反向的。 在另一个实施方案中,重组表达载体上的α链和β链基因的表达可以由同一个启动 子所驱动,例如编码单链嵌合T细胞受体的情况,α链的核苷酸序列和β链的核苷酸序列由 Furin-F2A多肽编码序列相连接。 在另一些实施方案中,重组表达载体除了包含α链和β链基因外,还可以包含其它 功能分子的编码序列。一个实施方案包括表达自发荧光蛋白(如GFP或其它荧光蛋白)以用 于体内追踪成像。另一个实施方案包括表达可诱导的自杀基因系统。 本发明对表达载体没有特别的限制,但可以是能在包括哺乳动物细胞(例如,人、 4 CN 111574616 A 说 明 书 3/9 页 猴、兔、大鼠、仓鼠或小鼠细胞)、植物细胞、酵母细胞、昆虫细胞和细菌细胞(如大肠杆菌 (E.coli))在内的真核或原核细胞内复制和/或表达多核苷酸的载体。较佳地,它可以是载 体,包括至少一选择性标记,可操作地连接到合适的启动子,以致可以在宿主细胞内表达多 核苷酸。例如,载体可以包括导入噬菌体、质粒、粘粒、微型染色体、病毒或反转录病毒载体 的多核苷酸。 (3)一种T细胞受体修饰的细胞,所述细胞的表面被(1)所述的T细胞受体修饰。 作为优选的实施方式,所述细胞包括原始T细胞或其前体细胞,NKT细胞,或T细胞 株。 所述“T细胞受体修饰”中的“修饰”是指,通过基因转染使细胞表达有本发明所述 的T细胞受体,即,所述T细胞受体通过跨膜区锚定在所修饰的细胞的细胞膜上,并具有识别 抗原多肽的功能。 (4)一种制备(3)所述的T细胞受体修饰的细胞的方法,包括以下步骤: 1)提供细胞; 2)提供(2)所述的核酸; 3)将所述核酸转染入所述细胞中。 作为一种可选择的实施方式,所述的细胞来自自体。 作为另一种可选择的实施方式,所述的细胞来自自体。 在本发明中,所述的细胞包括原始T细胞或其前体细胞、NKT细胞、或T细胞株。术语 “原始T细胞(naive T cell)”是指外周血中尚未被相应抗原活化的成熟T细胞。这些细胞可 以通过本领域已知的方法分离得到。例如,T细胞可以从不同组织器官获得,包括外周血、骨 髓、淋巴组织、脾脏、脐带血、肿瘤组织。作为一种可选择的实施方式,T细胞可以来自造血干 细胞(HSCs),包括来自骨髓、外周血或者脐带血,通过干细胞标记分子例如CD34而分离获 得。 作为另一种可选择的实施方式,T细胞可以来自诱导性多功能干细胞(iPS cells),包括把特定基因或特定基因产物导入体细胞,使该体细胞转化为干细胞后,体外诱 导分化成T细胞或其前体细胞。T细胞可以通过常用方法如密度梯度离心法而获得,密度梯 度离心法的例子包括Ficoll或者Percoll密度离心。 作为一种可选择的实施方式,是利用血浆分离置换法(apheresis)或白细胞去除 法(leukapheresis)从外周血获得富集的T细胞的产物。 作为另一种可选择的实施方式,是用抗体标记特定细胞群后,通过磁珠分离的方 式(如系统(Miltenyi Biotec))、或流式细胞分离的方式获得富集的CD8 或CD4 T细胞。 优选地,所述T细胞前体细胞为造血干细胞。可以将本发明所述TCR的编码基因直 接引入造血干细胞,然后转输到体内,进一步分化成为成熟T细胞;也可以将编码基因引入 在体外特定条件下由造血干细胞分化成熟的T细胞中。 作为一种可选择的实施方式,所述转染的方式为病毒载体转染的方式,包括但不 限于γ逆转录病毒载体或慢病毒载体。 作为另一种可选择的实施方式,所述转染的方式为化学方式,包括但不限于大分 子复合物、纳米胶囊、微球体、微珠、微团和脂质体。 作为另一种可选择的实施方式,所述转染的方式为物理方式,物理方式包括但不 5 CN 111574616 A 说 明 书 4/9 页 限于通过磷酸钙沉淀、脂质体、微注射、电穿孔、基因枪等途径把TCR基因以DNA或RNA的形式 导入细胞内。 (5)一种药物组合物,该药物组合物包括作为活性成分的根据(3)所述的T细胞受 体修饰的细胞,及药学上可接受的载体。药学上可接受的载体是指不会对生物体引起显著 刺激且不会消除所施用化合物的生物活性和性质的载体或稀释剂。 可用于将本发明组合物配制为液体溶液形式的药学上可接受的载体包括生理盐 水,无菌水,林格氏溶液,缓冲盐溶液,葡萄糖溶液,麦芽糊精溶液,甘油,乙醇,和其中两种 或更多种的混合物。如果需要,本发明的组合物也可含有其它常规添加剂,如抗氧化剂,缓 冲剂和抑菌剂。此外,本发明组合物还可包含稀释剂,分散剂,表面活性剂,粘合剂和润滑 剂,以将它配置成可注射制剂,如水性溶液,悬浮液和乳剂,丸剂,胶囊剂,颗粒剂和片剂。 药物组合物可以是各种口服或胃肠外制剂形式。使用包括填料,填充剂,粘合剂, 润湿剂,崩解剂,和表面活性剂在内的常规稀释剂或赋形剂配制药物组合物。固体口服制剂 包括片剂,丸剂,粉剂,颗粒剂,胶囊等。这些固体制剂可通过将至少一种化合物与一种或多 种赋形剂,例如,淀粉,碳酸钙,蔗糖,乳糖,明胶等混合来制备。除了简单的赋形剂,也可使 用润滑剂如硬脂酸镁或滑石。此外,液体口服制剂包括悬浮液,溶液,乳剂和糖浆等。除了通 常用作简单稀释剂的水和液体石蜡外,还可包括各种赋形剂,例如,润湿剂,甜味剂,香料, 防腐剂等。肠胃外给药的制剂包括灭菌水溶液,非水溶剂,悬浮剂,乳剂,冻干剂,栓剂等。丙 二醇,聚乙二醇,植物油如橄榄油,可注射酯如油酸乙酯等可以用作非水溶剂和悬浮剂。栓 剂主要成分可以包括witepsol,聚乙二醇,吐温61,可可脂,月桂脂,甘油明胶等。 药物组合物可具有选自下组的任意一种制剂:片剂,丸剂,粉末,颗粒,胶囊,悬浮 液,溶液,乳剂,糖浆,灭菌水溶液,非水溶液,悬浮液,乳液,冻干制剂和栓剂。 (6)(3)所述的T细胞受体修饰的细胞或(5)所述的药物组合物在制备用于治疗或 预防肿瘤和/或癌症、或用于检测宿主的肿瘤和/或癌症的产品中的用途。 附图说明 图1是TCR-T杀伤功能检测图。 具体的实施方式 以下通过例子的方式进一步解释或说明本发明的内容,但这些例子不应被理解为 对本发明的保护范围的限制。 以下除非特别说明,否则以下例子中所用实验方法均使用生物工程领域的常规实 验流程、操作、材料和条件进行。 实施例1高通量测序筛选TCR序列 1、RNA提取及质控 收集急性髓系白血病患者的外周血样本,患者无甲肝,乙肝,丙肝,戊肝,艾滋病, 梅毒,淋病和结核感染。 在5mL Ficoll中缓慢加入外周血,离心2000rpm,15min。吸取中间白膜层,加入 0.9%生理盐水,计数单个核细胞数量,离心1000rpm,5min,磁珠分选T细胞。采用TRIzol法 对处理的细胞样本进行RNA的提取,对提取后的RNA质量使用Qubit RNA HS Assay kits,经 2100生物分析仪(安捷伦)检测RNA完整性。 6 CN 111574616 A 说 明 书 5/9 页 2、反转录及文库制备 用Repertoire Analysis Kit(Human TCR alpha ,beta)进行建库。将所有试剂置 于冰上解冻,在配置mix之前,混匀和离心这些试剂。在冰上配置杂交引物需用的mix(表1)。 充分混匀后离心,加热反转录引物杂交mix,65℃5min,冰上孵育至少2min。在冰上准备配制 反转录mix(表2),混匀后离心mix。 表1反应体系 组分 体积 RT dNTP Mixture 1μl RT Primer H TCRα/β 1μl RNA 样本(100pg-1000ng) 最多到6.2μl Nuclease-free water 补足至8.2μl 表2反转录体系 组分 体积 RT buffer A 4μl RT buffer B 1μl RT buffer C 3.8μl RT Universal primer 1μl RNase inhibitor 1μl Reverse Transcriptase 1μl 总体积 11.8μl 将11 .8μl的杂交buffer加到上一步反应的杂交RNA中混匀,然后离心,在PCR仪 (T100,Bio-RAD)上运行以下程序(表3): 表3反应条件 3、第一步PCR 准备第一步PCR需用的试剂(表4),并在冰上解冻,混匀后瞬时离心,在冰上配制第 一步PCR反应的mix,配置好的mix用移液器混匀,然后离心。 表4第一步PCR反应体系 7 CN 111574616 A 说 明 书 6/9 页 每管中加入41μl的第一步PCR mix,加入9μl的第一链cDNA产物中混匀,然后离心, 在PCR仪(T100,Bio-RAD)上运行以下程序: 表5第一步PCR反应条件 4、第二步PCR 准备第二步PCR需用的试剂(表6),并在冰上解冻,混匀后瞬时离心,在冰上配制第 二步PCR反应的mix,配置好的mix用移液器混匀,然后离心。 表6第二步PCR反应体系 组分 体积 PCR buffer 25μl PCR dNTP Mixture 10μl Nuclease-free water 3μl DNA polymerase 1μl 总体积 39μl 准备一个新的PCR管,每管中加入1μl的第二步PCR引物,hTCRα#1-18(编号:A1- A18),或者hTCRβ#1-18(编号:B1-B18)。加入39μl第二步反应的mix和10μl的第一步PCR产物 混匀,然后离心,在PCR仪(T100,Bio-RAD)上运行以下程序: 8 CN 111574616 A 说 明 书 7/9 页 表7第二步PCR反应条件 5、第三步PCR 准备第三步PCR需用的试剂在冰上解冻(表9),混匀后瞬时离心。在冰上配制第二 步PCR反应的mix,配置好的mix用移液器混匀,然后离心。 表8第三步PCR反应体系 组分 体积 PCR buffer 25μl PCR dNTP Mixture 10μl 3rd universal primer 2.5μl Nuclease-free water 6.5μl DNA polymerase 1μl 总体积 45μl 准备一个新的PCR管,每管中加入45μl的第三步PCR mix,加入5μl的第二步PCR产 物中,用手指肚弹匀,然后离心,在PCR仪(T100,Bio-RAD)上运行以下程序: 表9第三步PCR反应条件 6、琼脂糖凝胶电泳 配置1.5%的琼脂糖胶,用1*TAE buffer和核酸染料(北京金博益),DNA marker上 样量为2μl,加1μl的6*loading buffer到PCR产物中,点样。100V电泳30-45min。使用凝胶到 成像系统(1708195,Bio-RAD),判断产物大小。hTCRɑ/β片段在650bp左右。 9 CN 111574616 A 说 明 书 8/9 页 7、用AGENCOURT AMPure XP(BEACKMAN)磁珠纯化 准备nuclease-free 0.2mL的8连管,按照表10稀释文库。 表10稀释体系 组分 体积 第三步PCR产物 30μl Nuclease-free water 20μl 总体积 50μl 配置DNase-free 70%乙醇(sigma)。磁珠使用前室温平衡30min,将22.5μl的磁珠 加到稀释后文库中,用移液器混匀至少10次。室温孵育5min,然后简单的离心。将8连管放置 在96孔磁力架上磁吸5min,观察液体和磁珠分离。将所有的上清转移到新的8连管中。再次 混匀未使用过的磁珠,加17.5μl的磁珠到上清中,用移液器混匀至少10次。室温孵育5min, 然后简单离心。将8连管放在96孔磁力架上磁吸5min,观察液体和磁珠分离。弃85μl的上清, 保留5μl的上清以免吸到磁珠。不要将磁珠与磁力架分离。加200μl的70%的乙醇漂洗。室温 30s,弃酒精,重复酒精洗涤步骤。弃所有上清,加30μl的10mM Tris-HCl到每个PCR管中,用 移液器混匀至少10次。室温孵育2min然后简单离心。将离心管放置在磁力架上室温5min,分 离液体和磁珠。将上清20μl转移至新的PCR管中。 8、文库浓度定量及质控 测定文库浓度用Qubit dsDNA HS kit(英潍捷基),使用设备Qubit 2.0(life),取 2μl的样本用于测定。通常文库浓度集中在5-40ng/μl。如果样本浓度≥1.72ng/μl可用于 Miseq测序。 9、文库目标片段质控 人的TCRα/β文库目标片段集中在650bp,使用1.5%的琼脂糖凝胶电泳对文库片段 进行质控,用1*TAE buffer和核酸染料(北京金博益),DNA marker上样量为2μl,加1μl的6* loading buffer到PCR产物中,点样。100V电泳30-45min。使用凝胶到成像系统(1708195, Bio-RAD),判断产物大小。 10、文库混库及质控 文库混样,是按此批次浓度最低的文库为标准,浓度最低文库乘以10μl为基准纳 克数,其他文库按照此纳克数进行取样,确保每个文库的总量是一致的,混样后按照纳克与 摩尔数之间的换算,稀释到8.58ng/μl(20nM,650bp)。 11、高通量测序 文库使用Miseq(Illumina)进行2×300bp双端测序,对上述混合完成的文库再次 使用设备Qubit 2.0(life)进行文库定量,最终稀释到10pM,与10pM denatured PhiX进行 混合(PhiX占比30%),混合后的600μl进行上机测序。 12、数据分析 采用MiXCR进行初级分析,可以对高度个性化的TCR和免疫球蛋白序列进行分析。 MiXCR可以针对不同的数据类型在参数上进行调整,并对分析结果和输出进行优化。进一步 高级分析多个多样性指数,如香农指数(Shannon)、辛普森指数(Simpson)、Inverse- Simpson指数和基尼指数(Gini)等。采用VDJtools用于二级TCR profiling分析以及多样性 评估。 10 CN 111574616 A 说 明 书 9/9 页 13、噬菌体展示技术筛选高亲和力的TCR序列。 14、结果 通过噬菌体展示技术筛选出高亲和力的TCR,其α链可变区的氨基酸序列如SEQ ID NO.4所示,其中CDR1-3的序列分别如SEQ ID NO.1-3所示;其β链可变区的氨基酸序列如SEQ ID NO .11-14任一项所示,其中,CDR1-2的序列分别如SEQ ID NO .5-6所示,CDR3的序列如 SEQ ID NO.7~10任一项所示。 实施例2 TCR-T的构建 1、利用高通量测序和数据分析结果,全合成相关序列,通过XbaI/SalI限制内切酶 切点,连接到pCDH载体中。 2、TCR-T细胞制备 采集健康人外周血,在Ficoll中缓慢加入外周血,离心2000rpm,15min。吸取中间 白膜层,加入0.9%生理盐水,计数单个核细胞数量,离心1000rpm,5min。磁珠分选T细胞。同 时加入CD3/CD28抗体偶联磁珠刺激,24h及48h后加入病毒感染2次,病毒感染时加入IL-2, 培养3-20天,获得TCR-T细胞。 实施例3 TCR-T杀伤功能检测 从本研究中所述的序列构建的TCR-T中任选一个进行功能检测。 计数靶细胞(急性髓系白血病细胞OCI-AMLP3)和阴性参照靶细胞(Daudi),分别标 记Celltrace far red和CFSE染色。计数TCR-T(TCR的Vβ可变区的氨基酸序列如SEQ ID NO.11所示)细胞作为效应细胞。按照计划效靶比(3:1,9:1,18:1),重悬效应细胞和靶细胞 至相应浓度。圆底96孔板中每个效靶比分别铺入铺入组1效应细胞、组2靶细胞和组3效应细 胞 靶细胞,每组4个复孔。培养2-24h,收细胞样本,分别收管A:组1效应细胞 组2靶细胞,管 B:组3效应细胞 靶细胞,多聚甲醛液固定,流式上机。作Killing Rate与E:T Ratio曲线图。 其中, 结果,如图1所示,相比对照组,本申请的TCR-T具有较好的杀伤效果。 上述实施例的说明只是用于理解本发明的方法及其核心思想。应当指出,对于本 领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进 和修饰,这些改进和修饰也将落入本发明权利要求的保护范围内。 11 CN 111574616 A 序 列 表 1/6 页 序列表 <110> 深圳豪石生物科技有限公司 <120> 分离的T细胞受体和应用 <160> 14 <170> SIPOSequenceListing 1.0 <210> 1 <211> 6 <212> PRT <213> 人工序列(Artificial Sequence) <400> 1 Val Ser Asn Ala Tyr Asn 1 5 <210> 2 <211> 4 <212> PRT <213> 人工序列(Artificial Sequence) <400> 2 Gly Ser Lys Pro 1 <210> 3 <211> 15 <212> PRT <213> 人工序列(Artificial Sequence) <400> 3 Cys Ala Val Asp Glu Asp Gln Thr Gly Ala Asn Asn Leu Phe Phe 1 5 10 15 <210> 4 <211> 109 <212> PRT <213> 人工序列(Artificial Sequence) <400> 4 Lys Asp Gln Val Phe Gln Pro Ser Thr Val Ala Ser Ser Glu Gly Ala 1 5 10 15 Val Val Glu Ile Phe Cys Asn His Ser Val Ser Asn Ala Tyr Asn Phe 20 25 30 Phe Trp Tyr Leu His Phe Pro Gly Cys Ala Pro Arg Leu Leu Val Lys 35 40 45 Gly Ser Lys Pro Ser Gln Gln Gly Arg Tyr Asn Met Thr Tyr Glu Arg 12 CN 111574616 A 序 列 表 2/6 页 50 55 60 Phe Ser Ser Ser Leu Leu Ile Leu Gln Val Arg Glu Ala Asp Ala Ala 65 70 75 80 Val Tyr Tyr Cys Ala Val Asp Glu Asp Gln Thr Gly Ala Asn Asn Leu 85 90 95 Phe Phe Gly Thr Gly Thr Arg Leu Thr Val Ile Pro Tyr 100 105 <210> 5 <211> 5 <212> PRT <213> 人工序列(Artificial Sequence) <400> 5 Lys Gly His Asp Arg 1 5 <210> 6 <211> 6 <212> PRT <213> 人工序列(Artificial Sequence) <400> 6 Ser Phe Asp Val Lys Asp 1 5 <210> 7 <211> 14 <212> PRT <213> 人工序列(Artificial Sequence) <400> 7 Cys Ala Thr Ser Asp Ala Ser Arg Thr Asp Thr Gln Tyr Phe 1 5 10 <210> 8 <211> 12 <212> PRT <213> 人工序列(Artificial Sequence) <400> 8 Cys Ala Thr Ser Pro Gln Gly Thr Glu Gln Phe Phe 1 5 10 <210> 9 <211> 13 <212> PRT <213> 人工序列(Artificial Sequence) 13 CN 111574616 A 序 列 表 3/6 页 <400> 9 Cys Ala Thr Ala Ser Gly Arg Gly Gly Glu Leu Phe Phe 1 5 10 <210> 10 <211> 14 <212> PRT <213> 人工序列(Artificial Sequence) <400> 10 Cys Ala Ile Arg Leu Ala Gly Gly Tyr His Glu Gln Phe Phe 1 5 10 <210> 11 <211> 174 <212> PRT <213> 人工序列(Artificial Sequence) <400> 11 Asp Ala Asp Val Thr Gln Thr Pro Arg Asn Arg Ile Thr Lys Thr Gly 1 5 10 15 Lys Arg Ile Met Leu Glu Cys Ser Gln Thr Lys Gly His Asp Arg Met 20 25 30 Tyr Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Leu Ile Tyr Tyr 35 40 45 Ser Phe Asp Val Lys Asp Ile Asn Lys Gly Glu Ile Ser Asp Gly Tyr 50 55 60 Ser Val Ser Arg Gln Ala Gln Ala Lys Phe Ser Leu Ser Leu Glu Ser 65 70 75 80 Ala Ile Pro Asn Gln Thr Ala Leu Tyr Phe Cys Ala Thr Ser Trp Tyr 85 90 95 Arg Gln Asp Pro Gly Leu Gly Leu Arg Leu Ile Tyr Tyr Ser Phe Asp 100 105 110 Val Lys Asp Ile Asn Lys Gly Glu Ile Ser Asp Gly Tyr Ser Val Ser 115 120 125 Arg Gln Ala Gln Ala Lys Phe Ser Leu Ser Leu Glu Ser Ala Ile Pro 130 135 140 Asn Gln Thr Ala Leu Tyr Phe Cys Ala Thr Ser Asp Ala Ser Arg Thr 145 150 155 160 Asp Thr Gln Tyr Phe Gly Ser Gly Thr Arg Leu Thr Val Val 165 170 <210> 12 <211> 172 14 CN 111574616 A 序 列 表 4/6 页 <212> PRT <213> 人工序列(Artificial Sequence) <400> 12 Asp Ala Asp Val Thr Gln Thr Pro Arg Asn Arg Ile Thr Lys Thr Gly 1 5 10 15 Lys Arg Ile Met Leu Glu Cys Ser Gln Thr Lys Gly His Asp Arg Met 20 25 30 Tyr Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Leu Ile Tyr Tyr 35 40 45 Ser Phe Asp Val Lys Asp Ile Asn Lys Gly Glu Ile Ser Asp Gly Tyr 50 55 60 Ser Val Ser Arg Gln Ala Gln Ala Lys Phe Ser Leu Ser Leu Glu Ser 65 70 75 80 Ala Ile Pro Asn Gln Thr Ala Leu Tyr Phe Cys Ala Thr Ser Trp Tyr 85 90 95 Arg Gln Asp Pro Gly Leu Gly Leu Arg Leu Ile Tyr Tyr Ser Phe Asp 100 105 110 Val Lys Asp Ile Asn Lys Gly Glu Ile Ser Asp Gly Tyr Ser Val Ser 115 120 125 Arg Gln Ala Gln Ala Lys Phe Ser Leu Ser Leu Glu Ser Ala Ile Pro 130 135 140 Asn Gln Thr Ala Leu Tyr Phe Cys Ala Thr Ser Pro Gln Gly Thr Glu 145 150 155 160 Gln Phe Phe Gly Ser Gly Thr Arg Leu Thr Val Val 165 170 <210> 13 <211> 173 <212> PRT <213> 人工序列(Artificial Sequence) <400> 13 Asp Ala Asp Val Thr Gln Thr Pro Arg Asn Arg Ile Thr Lys Thr Gly 1 5 10 15 Lys Arg Ile Met Leu Glu Cys Ser Gln Thr Lys Gly His Asp Arg Met 20 25 30 Tyr Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Leu Ile Tyr Tyr 35 40 45 Ser Phe Asp Val Lys Asp Ile Asn Lys Gly Glu Ile Ser Asp Gly Tyr 50 55 60 Ser Val Ser Arg Gln Ala Gln Ala Lys Phe Ser Leu Ser Leu Glu Ser 15 CN 111574616 A 序 列 表 5/6 页 65 70 75 80 Ala Ile Pro Asn Gln Thr Ala Leu Tyr Phe Cys Ala Thr Ser Trp Tyr 85 90 95 Arg Gln Asp Pro Gly Leu Gly Leu Arg Leu Ile Tyr Tyr Ser Phe Asp 100 105 110 Val Lys Asp Ile Asn Lys Gly Glu Ile Ser Asp Gly Tyr Ser Val Ser 115 120 125 Arg Gln Ala Gln Ala Lys Phe Ser Leu Ser Leu Glu Ser Ala Ile Pro 130 135 140 Asn Gln Thr Ala Leu Tyr Phe Cys Ala Thr Ala Ser Gly Arg Gly Gly 145 150 155 160 Glu Leu Phe Phe Gly Ser Gly Thr Arg Leu Thr Val Val 165 170 <210> 14 <211> 174 <212> PRT <213> 人工序列(Artificial Sequence) <400> 14 Asp Ala Asp Val Thr Gln Thr Pro Arg Asn Arg Ile Thr Lys Thr Gly 1 5 10 15 Lys Arg Ile Met Leu Glu Cys Ser Gln Thr Lys Gly His Asp Arg Met 20 25 30 Tyr Trp Tyr Arg Gln Asp Pro Gly Leu Gly Leu Arg Leu Ile Tyr Tyr 35 40 45 Ser Phe Asp Val Lys Asp Ile Asn Lys Gly Glu Ile Ser Asp Gly Tyr 50 55 60 Ser Val Ser Arg Gln Ala Gln Ala Lys Phe Ser Leu Ser Leu Glu Ser 65 70 75 80 Ala Ile Pro Asn Gln Thr Ala Leu Tyr Phe Cys Ala Thr Ser Trp Tyr 85 90 95 Arg Gln Asp Pro Gly Leu Gly Leu Arg Leu Ile Tyr Tyr Ser Phe Asp 100 105 110 Val Lys Asp Ile Asn Lys Gly Glu Ile Ser Asp Gly Tyr Ser Val Ser 115 120 125 Arg Gln Ala Gln Ala Lys Phe Ser Leu Ser Leu Glu Ser Ala Ile Pro 130 135 140 Asn Gln Thr Ala Leu Tyr Phe Cys Ala Ile Arg Leu Ala Gly Gly Tyr 145 150 155 160 His Glu Gln Phe Phe Gly Ser Gly Thr Arg Leu Thr Val Val 16 CN 111574616 A 序 列 表 6/6 页 165 170 17 CN 111574616 A 说 明 书 附 图 1/1 页 图1 18












