技术摘要:
本发明涉及一种三疣梭子蟹原肌球蛋白过敏检测试剂的应用,检测试剂包括PCR扩增引物,其中,上游引物F为:5’‑CATATGAAGAAGATGCAGC AGGTTGAGAA‑3’;下游引物R为:5’‑CTCGAGTTAGTGGTGGTGGTGGTGGTGATAGCCAGACAGTTCGCTGAACGT‑3’。通过基因库获得三疣梭子蟹原肌球蛋 全部
背景技术:
食物过敏是机体的免疫系统对食物过敏原蛋白产生的特异性反应。目前,食物过 敏的体外检测常采用酶联免疫吸附检测法。传统的食物过敏酶联免疫检测法分为两种,一 种是利用抗过敏原抗体来检测样本中的食物过敏原,另一种是通过天然的食物总蛋白作为 抗原来检测样本中的特异性IgE抗体。前一种检测方法需要大量高度纯化的抗体,而抗体的 制备耗时较长,产量较少。后一种检测方法则无法人为地控制蛋白的纯度等因素,增加了食 物过敏检测的假阴性和假阳性率,降低了检测的准确性。目前,一种新型过敏原检测方 法——单组分诊断(component resolved diagnosis,CRD)被广泛认识,该方法利用提取获 得的天然过敏原组分或重组表达获得的过敏原作为已知抗原来检测对该过敏组分过敏的 疾病。与传统的利用食物总蛋白提取物为抗原的方法相比,CRD可以有目的性地分析天然总 蛋白中含量较少的非主要过敏原,重组的过敏单组分可以人为地控制质量、纯度、产量等影 响因素。 甲壳类动物及其制品是联合国粮农组织提出的八大类引起过敏的食物之一。三疣 梭子蟹是重要的渔业资源,部分消费者食用后会有过敏反应。关于蟹类过敏原的检测主要 是采用ImmunoCAP250过敏原检测系统(刘平,陶淇惠,李志艳,等.2013至2017年11641例患 者常见过敏原流行特征分析[J] .中华检验医学杂志,2019,42(5):371-374 .)、欧蒙公司 EIROLineScan系统(钟丽红,丘创华,李卓成,等。过敏性疾病患者血清IgE和细胞结合IgE水 平变化及临床意义[J].深圳中西医结合杂志,2019,29(7):12-15.)和DX-Blot 45型过敏原 检测系统(周琼艳,林薇,许素玲,李澍铖,袁波,彭岚,赵可喻,郭小燕.嗜酸性粒细胞和IgE 在过敏性皮肤病中的意义[J].现代实用医学,2020,32(2):198-200.)等,但这些系统没有 特别针对三疣梭子蟹过敏原检测。原肌球蛋白(Tropomyosin,TM)是三疣梭子蟹的主要过敏 原之一,原肌球蛋白的含量较大。而现有技术还没有关于三疣梭子蟹原肌球蛋白过敏检测 试剂相关的报道,这使得针对三疣梭子蟹原肌球蛋白过敏疾病的防控和治疗比较有限。
技术实现要素:
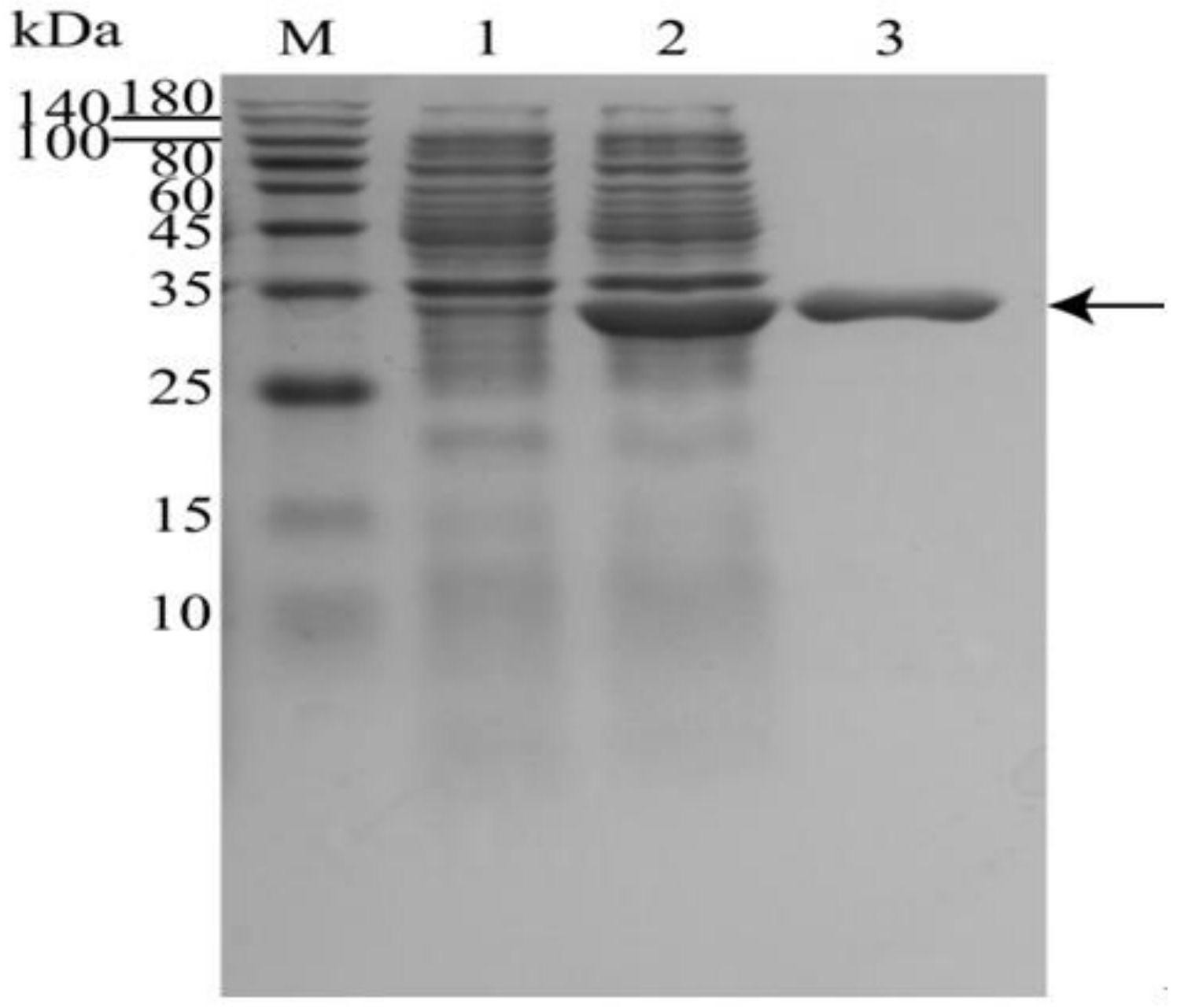
本发明所要解决的技术问题是针对现有技术的现状而提出一种三疣梭子蟹原肌 球蛋白过敏检测试剂的应用。 本发明解决上述技术问题所采用的技术方案为:一种三疣梭子蟹原肌球蛋白过敏 检测试剂的应用,其特征在于:检测试剂包括PCR扩增引物,其中, 上游引物F为: 5’-CATATGAAGAAGATGCAGCAGGTTGAGAA-3’; 下游引物R为: 3 CN 111596070 A 说 明 书 2/7 页 5’-CTCGAGTTAGTGGTGGTGGTGGTGGTGATAGCCAGACAGTTCGCTGAACGT-3’。 进一步地,所述检测试剂包括ELISA检测试剂。 一种制备三疣梭子蟹重组原肌球蛋白的方法,其特征在于:包括以下步骤: 1)从现有数据库里获得三疣梭子蟹原肌球蛋白的基因序列; 2)以步骤1)的基因序列,设计扩增引物,进行扩增; 3)将步骤2)扩增后的目的基因连接到原核表达载体中,构建重组质粒; 4)将步骤3)构建的所述重组质粒转入宿主菌,诱导其表达蛋白; 5)将步骤4)获得的蛋白经纯化而获得三疣梭子蟹重组原肌球蛋白。 进一步地,在所述步骤2)中,PCR扩增的引物为: 上游引物F为: 5’-CATATGAAGAAGATGCAGCAGGTTGAGAA-3’; 下游引物R为: 5’-CTCGAGTTAGTGGTGGTGGTGGTGGTGATAGCCAGACAGTTCGCTGAACGT-3’。 一种三疣梭子蟹重组原肌球蛋白,其特征在于:该三疣梭子蟹重组原肌球蛋白的 氨基酸序列为: Met Lys Lys Met Gln Gln Val Glu Asn Glu Leu Asp Gln Ala Gln Glu Gln Leu Ser Ala Ala Asn Thr Lys Leu Asp Glu Lys Glu Lys Ala Leu Gln Asn Ala Glu Gly Glu Val Ala Ala Leu Asn Arg Arg Ile Gln Leu Leu Glu Glu Asp Leu Glu Arg Ser Glu Glu Arg Leu Asn Thr Ala Thr Thr Lys Leu Ala Glu Ala Ser Gln Ala Ala Asp Glu Ser Glu Arg Met Arg Lys Val Leu Glu Asn Arg Ser Leu Ser Asp Glu Glu Arg Met Asp Ala Leu Glu Asn Gln Leu Lys Glu Ala Arg Phe Leu Ala Glu Glu Ala Asp Arg Lys Tyr Asp Glu Val Ala Arg Lys Leu Ala Met Val Glu Ala Asp Leu Glu Arg Ala Glu Glu Arg Ala Glu Ser Gly Glu Ser Lys Ile Val Glu Leu Glu Glu Glu Leu Arg Val Val Gly Asn Asn Leu Lys Ser Leu Glu Val Ser Glu Glu Lys Ala Asn Gln Arg Glu Glu Thr Tyr Lys Glu Gln Ile Lys Thr Leu Ala Asn Lys Leu Lys Ala Ala Glu Ala Arg Ala Glu Phe Ala Glu Arg Ser Val Gln Lys Leu Gln Lys Glu Val Asp Arg Leu Glu Asp Glu Leu Val Asn Glu Lys Glu Lys Tyr Lys Ser Ile Thr Asp Glu Leu Asp Gln Thr Phe Ser Glu Leu Ser Gly Tyr His His His His His His。 与现有技术相比,本发明的优点在于:通过基因库获得三疣梭子蟹原肌球蛋白的 编码基因片段;将致敏原基因片段克隆至原核表达载体中,构建重组表达质粒,再转入宿主 菌中诱导其表达,采用亲和层析方法纯化,从而获得重组三疣梭子蟹原肌球蛋白;该蛋白可 与三疣梭子蟹过敏患者血清的特异性IgE结合,从而可用于临床诊断及致敏原组分筛查。 附图说明 图1为本发明实施例二中重组质粒pMD-19T-TM的双酶切鉴定结果图(M表示 DNAMarker;泳道1表示未酶切的质粒;泳道2、泳道3分别表示酶切后的质粒); 图2为本发明实施例二中表达载体pET-21a( )的双酶切鉴定结果图(M表示 DNAMarker;泳道1表示未酶切的质粒;泳道2、泳道3分别表示酶切后的质粒); 图3为本发明实施例二中重组质粒pET-21a( )-TM的菌液PCR验证图(M表示 4 CN 111596070 A 说 明 书 3/7 页 DNAMarker;泳道1-5表示随机挑取的单菌落PCR产物); 图4为本发明实施例二中重组的原肌球蛋白的SDS-PAGE验证图(M表示蛋白标准 Marker;泳道1表示未加IPTG诱导的重组蛋白;泳道2表示IPTG诱导5h后未纯化的重组蛋白; 泳道3表示IPTG诱导5h后纯化的重组蛋白); 图5为本发明实施例三中三疣梭子蟹重组原肌球蛋白在不同浓度包被的ELISA试 剂检测结果; 图6为本发明实施例三中不同包被条件下蟹过敏阳性血清与阴性血清的ELISA试 剂检测结果(1表示第一组的处理条件37℃包被3h,4℃包被12h;2表示第二组的处理条件37 ℃包被3h;3表示第三组的处理条件4℃包被12h); 图7为本发明实施例三中不同封闭条件下蟹过敏阳性血清与阴性血清的ELISA试 剂检测结果(1表示第一组的处理条件为37℃包被3h,4℃包被12h;2表示第二组的处理条件 37℃包被3h;3表示第三组的处理条件4℃包被12h); 图8为本发明实施例三中重组原肌球蛋白检测三疣梭子蟹过敏的ROC曲线。












