技术摘要:
本发明涉及一种单克隆抗体对帕金森病的治疗作用,所述单克隆抗体为抗丝氨酸129位磷酸化alpha突触核蛋白(p‑α‑synuclein,p‑α‑syn)单克隆抗体(C140S),本发明特别涉及此抗体在治疗免疫细胞异常激活的作用研究。
背景技术:
帕金森病(Parkinson`s Disease,PD)是一种常见的神经退行性疾病,主要表现为 行动迟缓、肌僵直、静止性震颤和姿势不稳等运动症状,同时其他神经调节和神经递质系统 也受到影响,导致各种非运动性症状,例如认知能力降低、抑郁、睡眠紊乱、嗅觉障碍,排尿 和胃肠道异常等症状;帕金森病的发病机制尚不完全清楚,主要病理学特征是在中脑黑质 中多巴胺能神经元细胞进行性死亡,在神经细胞中α-突触核蛋白(α-syn)聚集形成路易小 体,其主要成分为丝氨酸129位磷酸化alpha突触核蛋白(p-α-syn)。 PD目前的治疗方法主要是药物治疗,药物治疗中最经典药物的是左旋多巴,但是 左旋多巴只能改善运动症状,此类药物随着使用时间的延长和剂量增大,毒副作用越来越 大,大多数PD患者出现疗效减退和“开-关”现象,另一类药物是酶的抑制剂比如MAO-B抑制 剂,可以通过特异性抑制单胺氧化酶B起到减少多巴胺代谢的作用,但是部分患者会出现不 自主运动等副作用。深部脑刺激(DBS)治疗是针对病人的震颤症状,使用一定频率的电信号 刺激丘脑底核,从而起到缓解运动障碍的目的。这些治疗方法均是针对运动症状的治疗,无 法真正延缓疾病的进程,并且对于疾病的适应症有一定的局限性,因此针对病因特异性较 强的免疫疗法显示出它的优势。抗体作为药物可以靶向识别引起疾病发生的目标蛋白,促 进目标蛋白清除,减少目标蛋白聚集和阻止目标蛋白的传播从而起到治疗的作用。 对于帕金森病来说免疫疗法治疗的目标蛋白就是α-突触核蛋白。α-突触核蛋白异 常的聚集形式以及磷酸化修饰都可以引起细胞毒性,并在细胞间传播,进而引起细胞死亡, 引发帕金森病。目前针对α-syn的抗体有针对不同聚集状态的α-syn的抗体(抗单体,抗寡聚 体,抗纤维化抗体);α-syn分为三个结构域,N端,NAC区及C端,所以也有针对识别α-syn不同 区域的抗体(抗N端,抗C端,抗NAC区抗体),但是目前均没有应用到临床上。而α-突触核蛋白 发挥毒性作用主要与它的磷酸化修饰有关,丝氨酸129位磷酸化的alpha突触核蛋白对细胞 的损伤更大,更其易于聚集和传播,使其更难被降解,从而引起细胞毒性和神经退行性变 化。使用特异抗丝氨酸129位磷酸化alpha突触核蛋白单克隆抗体中和毒性蛋白,从而减轻 其细胞毒性是一种新的针对病因的治疗方法。 抗丝氨酸129位磷酸化alpha突触核蛋白(p-α-synuclein ,p-α-syn)单克隆抗体 (简称:C140S):公开在中国专利ZL201610913085.1中,该专利说明书中描述了该抗体的来 源:为建立本发明所述的ELISA检测方法,特制备了一种针对129位磷酸化的人源α-syn的小 鼠源单克隆抗体C140S,该单克隆抗体的制备方法如下:使用P1(M18631-1hz-1-1 ,Ac- CEAYEMP(pS)EGG-NH2,人源129位丝氨酸磷酸化α-syn的123-131肽段)肽段免疫balb-c小 鼠,取脾制备融合骨髓瘤细胞系,间接法ELISA筛选出克隆号为C140S的细胞系,使用该细胞 3 CN 111544584 A 说 明 书 2/9 页 系注射入4只balb-c/nu小鼠腹腔,间接法ELISA验证腹水反应特异性后纯化抗体,再次使用 间接法ELISA验证纯化的抗体的反应性后(即0.125ug/ml的抗体识别1000ng/ml的阳性组 490nm波长吸光光度值高于阴性组至少30倍,且背景和阴性组读数小于0.2),方可用作本方 法中的检测抗体,最终浓度为4mg/ml。 (该细胞株已经保藏在中国普通微生物菌种保藏管理中心,编号为CGMCC12993,保 藏日期16年9月26日,分类命名:抗体杂交瘤细胞,地址北京市朝阳区北辰西路1号院3号)。
技术实现要素:
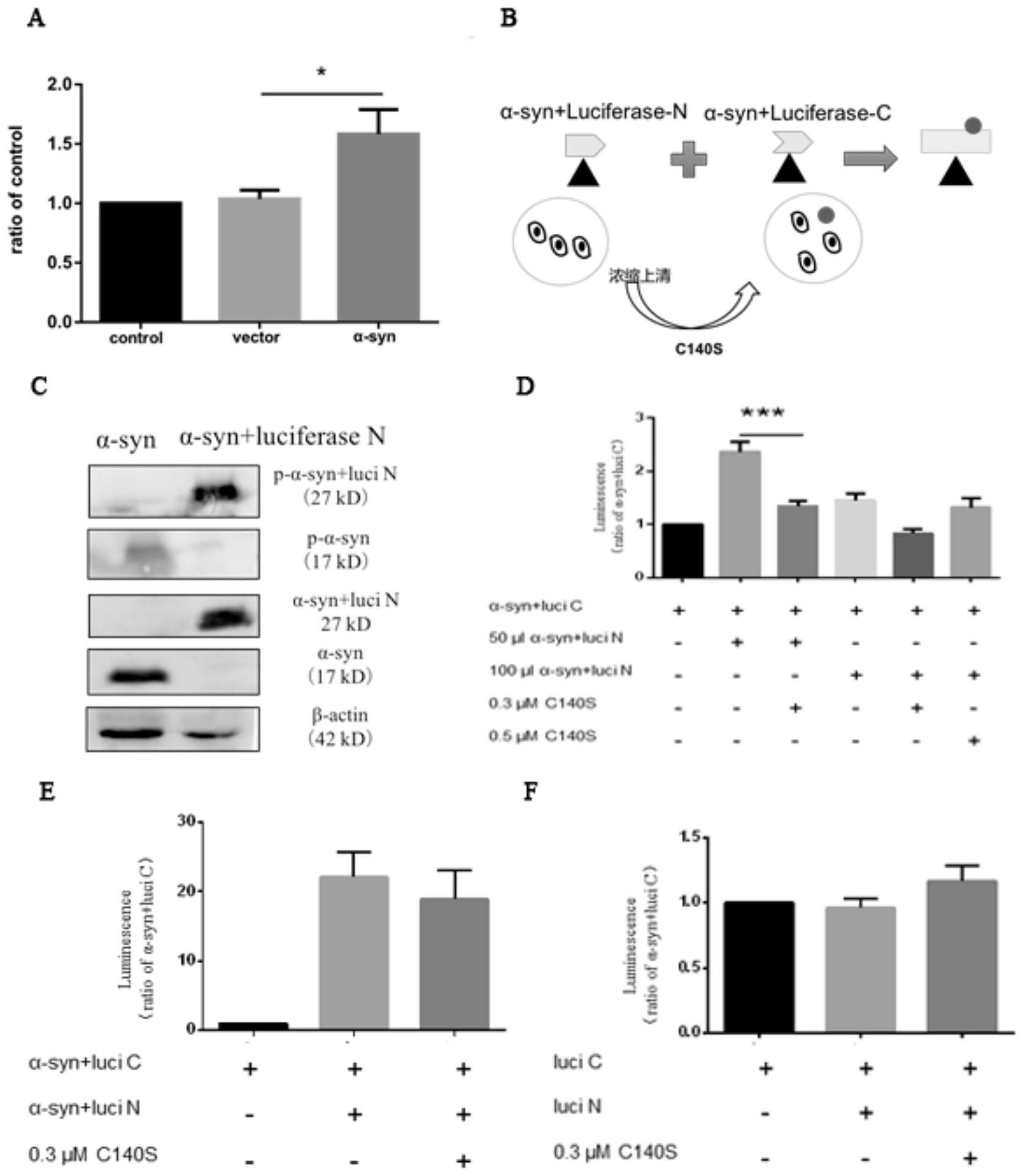
本发明提供一种抗丝氨酸129位磷酸化alpha突触核蛋白单克隆抗体(C140S)在制 备治疗帕金森病的药物中的应用,其中所述应用基于该抗体可以阻断p-α-syn在细胞间传 播。 本发明为此进一步提供一种药物制剂,其包含抗丝氨酸129位磷酸化alpha突触核 蛋白单克隆抗体(C140S),其中所述单克隆抗体,类型为:IgG,此抗体亚型为:IgG2b。所述药 物制剂,可以以任何方式施用于哺乳动物,包括人。优选采用非胃肠道方法给药,特别优选 的是注射方式给药。 本发明所述的应用,为所述抗体可以阻断p-α-syn在细胞间传播。 本发明所述的应用,为所述抗体在6小时即可以通过血脑屏障进入脑实质内。 本发明所述的应用,为所述抗体可以改善CD4 /CD8 T细胞的比例倒置,能缓解转 基因小鼠的行为障碍,增加转基因小鼠的转棒停留时间,增加小鼠的四肢力量,增强转基因 小鼠的协调能力。 本发明所述的应用,为所述抗体可以中和毒性蛋白,减轻其细胞毒性。 本发明所述的应用,为所述抗体可以减少转基因动物脑内的p-α-syn含量,增加脑 内TH含量,缓解转基因小鼠的趋避性障碍,说明此抗体C140S有神经保护作用,并对PD模型 有治疗作用。 为证明本发明的用途,本发明以抗丝氨酸129位磷酸化alpha突触核蛋白单克隆抗 体(C140S)为实验药物,对有关帕金森病模型进行了研究,研究结果如下: 采用的细胞模型为过表达α-syn的HEK293T细胞系。 具体步骤如下: 1)将α-syn基因转染进入HEK293T细胞中,24h后收集细胞上清进行间接法ELISA实 验,结果证明细胞上清中有分泌出的p-α-syn。 2)Luciferase的N端和C端聚集后会引起腔肠素发出荧光的特点,将Luciferase的 N段和C段分别与α-syn相连后分别转染进入HEK293T细胞中,24h后收集转染α-syn- luciferase-N培养基上清,加入到转染α-syn-luciferase-C的细胞培养基中,24h后使用腔 肠素显色,结果证明p-α-syn能在细胞间传播。 3)在α-syn-luciferase-N培养基上清中加入C140S后,转染α-syn-luciferase-C 质粒的细胞内荧光强度明显下降,说明C140S在p-α-syn传播过程中发挥了阻断作用。 本发明进一步提供抗丝氨酸129位磷酸化alpha突触核蛋白单克隆抗体(C140S)治 疗PD转基因动物模型的方法。 本发明采用的PD动物模型为过表达α-syn的转基因动物。 4 CN 111544584 A 说 明 书 3/9 页 具体步骤如下: 1)野生型小鼠腹腔注射罗丹明标记的C140S后,使用小鼠活体成像检测小鼠脑内 荧光强度,结果证明带有罗丹明标签的抗体药物C140S在6小时即可以通过血脑屏障进入脑 实质内。 2)转基因小鼠腹腔注射10mg/kg抗体C140S药物一周后,使用流式细胞仪检测各组 小鼠血浆中CD4 /CD8 T细胞的比例,结果证明抗体药物C140S可以改善CD4 /CD8 T细胞的比 例倒置,能缓解转基因小鼠的行为障碍,增加转基因小鼠的转棒停留时间,增加小鼠的四肢 力量,增强转基因小鼠的协调能力。 3)转基因小鼠脑立体定位注射C140S抗体至背侧纹状体,检测小鼠脑内p-α-syn和 酪氨酸羟化酶(TH)含量以及小鼠的运动行为。结果证明抗体药物C140S可以减少转基因动 物脑内的p-α-syn含量,增加脑内TH含量,缓解转基因小鼠的趋避性障碍,说明此抗体C140S 有神经保护作用,并对PD模型有一定治疗作用。 本发明的优点在PD动物模型腹腔注射C140S抗体药物后,能缓解外周血中免疫异 常的变化,脑立体定位注射抗体C140S于纹状体后,不仅能缓解PD模型的病理症状,还能缓 解转小鼠的运动行为障碍。 附图说明: 图1 P-α-syn可以在细胞间传播,使用抗体药物C140S可以阻断其传播过程。向 HEK293T细胞中转染α-syn质粒,24h收集细胞上清,浓缩10倍后行ELISA检测,结果显示过表 达α-syn组上清中α-syn明显多于对照组;B.将luciferase拆分为N端和C端,分别与α-syn相 连然后经过质粒转染进入HEK293T细胞中,收集α-syn luciferase-N端组上清浓缩后加入 α-syn luciferase-C端组中,24h后加入腔肠素,在酶标仪下检测自发荧光强度;C.收集转 染α-syn luciferase-N端细胞蛋白质,使用WB实验检测细胞中表达了α-syn蛋白和磷酸化 α-syn蛋白(17kd),同时也表达α-syn luciferase-N和磷酸化α-syn luciferase-N蛋白 (27kd);D.使用酶标仪检测自发荧光,发现向转染α-syn luciferase-C端组细胞中加入50μ l浓缩α-syn luciferase-N端组细胞上清,加入腔肠素后荧光强度明显升高,在浓缩上清中 加入磷酸化α-syn抗体c140s可以中和传播过程中p-α-syn luciferase-N,荧光强度明显下 降,加入其他体积浓缩上清和抗体差异不明显;E .向HEK293T细胞中同时转染α-syn luciferase-C和α-syn luciferase-N,使用腔肠素显色后荧光强度明显升高,此时在细胞 上清中加入C140S抗体不影响luciferase发光;F .由于缺少α-syn的聚集特性,仅转染 luciferase-N端和C端不能发出荧光。 图2:抗体C140S在小鼠体内半衰期为5天,腹腔注射可以减少转基因小鼠外周血中 p-α-syn的含量。A.向TG小鼠腹腔中注射10mg/kg的p-α-syn抗体药物(C140S),分别于第1, 3,5,7,9天取外周血使用ELISA法检测血液中C140S和p-α-syn的量;(B,C)用药后第9天后外 周血中p-α-syn量明显减少。 图3:腹腔注射抗体C140S可以缓解转基因小鼠体内异常的免疫反应。 A:取转基因动物外周血浆CD4 /CD8 细胞比例比野生型小鼠降低;B,C:腹腔注射 (INTRA)10mg/kg抗体C140S一周后,外周血浆中CD8 T细胞数量明显降低,CD4 /CD8 比例显 著升高。 5 CN 111544584 A 说 明 书 4/9 页 图4:腹腔注射抗体C140S可以通过转基因小鼠血脑屏障。将罗丹明作为荧光标签 与C140S抗体偶联并行腹腔注射后,A:活体检测小鼠体内C140S扩散程度;B:分别取4h,5h, 6h的小鼠脑冲血后进行成像,发现4h时带有罗丹明标签的C140S已经扩散至脑实质,而且随 着时间增长进入脑部的药物量逐渐增多。 图5:脑定位注射C140S后转基因小鼠外周血和脑实质的p-α-syn减少,小鼠脑内TH 阳性神经元丢失减少。A:注射C140S药物侧TH阳性神经元数量明显多于对照侧;B:立体定位 注射市售α-syn抗体作为对照抗体,C140S作为实验组进行抗体药物治疗后提取纹体可溶蛋 白质进行Western blot实验;C,D:结果发现TG组TH表达量与WT组相比明显减少,注射C140S 抗体药物组TH蛋白表达量明显多于TG组,而对照α-syn抗体组的TH表达量与TG组相比无明 显差异。 图6:脑定位注射C140S后转基因小鼠纹体内p-α-syn显著减少。A:分别提取可溶和 不可溶蛋白组分,进行Western blot实验;B,C:TG组经C140S治疗后可溶和不可溶蛋白组分 p-α-syn含量明显少于TG组,而α-syn抗体注射不能减少p-α-syn含量。 图7:C140S治疗可以缓解转基因小鼠的运动障碍 A.使用10-12月龄的小鼠进行转棒疲劳试验,做速度10-60r/min的加速运动,记录 运动时间发现TG小鼠转棒时间136±4.427秒,与WT组转棒时间166.2±6.339秒相比明显下 降,经过腹腔注射给药的动物转棒时间152.1±5.123秒与TG组相比有明显差异,说明有治 疗效果;B.使用10-12月龄小鼠进行旷场实验,正常小鼠会畏惧开阔场所而更愿意贴墙行 走,统计后发现TG组小鼠在周边区域停留时间占总活动时间的比约为0.81±0.01明显低于 WT组的0.98±0.02,说明其趋避性发生改变,经过立体定位注射抗体治疗后趋避性有所改 善,时间占比为0.96±0.03,与TG组相比提升明显;C.使用10-12月龄小鼠进行钻网实验评 价四肢力量,按照评分表进行打分,向上钻网成功 3分,四肢抓网10秒 2分,双前肢抓网10 秒 1分,10秒内掉落为0分,统计后发现TG组得分2.333±0 .4216分,明显低于WT组5± 0.4472分,而腹腔给药治疗组的2.833±0.4773分,与TG组相比无差别,说明四肢力量没有 出现恢复;D.使用10-12月龄小鼠进行爬杆实验评价其协调能力,统计发现TG组小鼠从顶端 爬到底端用时16.23±2.684秒,明显高于WT组8.39±1 .438秒,腹腔给药治疗组所用时间 11.62±1.596秒与TG组相比没有差异。












