技术摘要:
本申请提供儿童血液肿瘤患者脓毒性休克预测方法、装置、终端及介质,旨在利用医院电子病历信息库,结合机器学习的方法,建立脓毒性休克的机器学习模型,并将模型嵌入医生工作站的临床辅助决策系统(CDSS),对住院患儿实施实时监控,早期识别脓毒性休克高危患儿,以给予 全部
背景技术:
粒缺、发热的儿童血液肿瘤患者由于免疫功能低下,炎症的症状和体征常不明显, 病原菌及感染灶不明确,发热可能是感染的唯征象,如没有给予及时恰当的抗菌药物治疗, 感染相关死亡率高。国内外研究均发现,中性粒细胞减少和发热的儿童癌症患者中感染性 休克发生率为6~7%。儿童急性淋巴细胞白血病(ALL)中3%的患者发生治疗相关的死亡, 其中感染是最常见死因。因此,对于脓毒症休克人群的早期识别、提早诊断方法以及治疗, 对于降低脓毒性休克的发生和死亡风险至关重要。 虽然许多研究发现的脓毒性休克高危因素可以预测脓毒性休克的发生,例如免疫 抑制、长期化疗所致的血象变化、生命体征等,但是缺乏一个良好的量化模型来指导风险分 级。在成人脓毒症、脓毒性休克领域存在运用机器学习技术的临床模型被建立及验证,但尚 无针对儿童血液肿瘤粒缺发热患儿的菌血症、脓毒症相关的模型建立,更没有针对中国儿 童血液肿瘤粒缺/发热患者且便于临床使用的的脓毒性休克模型建立。 申请内容 鉴于以上所述现有技术的缺点,本申请的目的在于提供方法、装置、终端及介质, 用于解决现有技术中的问题。 为实现上述目的及其他相关目的,本申请的第一方面提供一种儿童血液肿瘤患者 脓毒性休克预测方法,包括:构建儿童血液肿瘤患者脓毒性休克数据集,据以构建儿童血液 肿瘤患者脓毒性休克预测模型;训练所述儿童血液肿瘤患者脓毒性休克预测模型并进行准 确性测试,并根据准确性测试结果选取最优预测模型;将所述最优预测模型适配于医疗应 用端中的临床辅助决策系统,并在待诊患者符合预设触发条件时,利用所述最优预测模型 对所述待诊患者进行诊断,并输出至少包括儿童血液肿瘤患者脓毒性休克信息的预测结 果。 于本申请的第一方面的一些实施例中,所述儿童血液肿瘤患者脓毒性休克预测模 型的构建方式包括:根据预设条件选取样本人群并采集源数据;从所述源数据中抽取病例 组和对照组并进行预处理;基于预处理后的数据,选取入模特征变量并构建儿童血液肿瘤 患者脓毒性休克预测模型。 于本申请的第一方面的一些实施例中,所述入模特征变量包括:呼吸频率、脉搏、 体温、C-反应蛋白、白细胞计数、谷丙转氨酶、活化部分凝血活酶时间、淋巴细胞占白细胞百 分比、平均红细胞体积、嗜碱性粒细胞计数、血钾、血小板计数、中性粒细胞计数、自由钙浓 度。 于本申请的第一方面的一些实施例中,每个所述入模特征变量有多个取值,所述 方法还包括基于时间窗对所述入模特征变量进行聚合衍生处理,以获取单个入模特征变量 4 CN 111599466 A 说 明 书 2/9 页 的多个取值之间的关联关系。 于本申请的第一方面的一些实施例中,所述聚合衍生处理的方式包括:有无预测、 计数、取最大值、取最小值、取平均值、取最末值、取最早值、取平均发展速度值、取标准差 值、取最大增幅值中的任意一种或多种的组合。 于本申请的第一方面的一些实施例中,所述单个入模特征变量的多个取值之间的 关联关系包括多个取值之间的变换、趋势、分布关系中的任意一种或多种的组合。 于本申请的第一方面的一些实施例中,对儿童血液肿瘤患者脓毒性休克预测模型 进行准确性测试的方式包括:计算每个模型的AUC值,并取AUC值最大的预测模型作为所述 最优预测模型。 于本申请的第一方面的一些实施例中,所述预设触发条件包括:年龄≤18岁的儿 童血液肿瘤科住院患者,且患者的ANC<1000/μl或者体温>38℃。 于本申请的第一方面的一些实施例中,所述预测模型的输出结果包括:儿童血液 肿瘤患者脓毒性休克的预测信息(如得分和危险级别等)、关键变量、保护因素和危险因素、 一时间段内预测信息的趋势、模型说明;其中,所述模型说明包括适用人群说明、模型启动 条件说明、预测结果含义的解释说明、阈值含义的解释说明。 为实现上述目的及其他相关目的,本申请的第二方面提供一种儿童血液肿瘤患者 脓毒性休克预测装置,包括:模型构建模块,用于构建儿童血液肿瘤患者脓毒性休克数据 集,据以构建儿童血液肿瘤患者脓毒性休克预测模型;模型测试模块,用于训练所述儿童血 液肿瘤患者脓毒性休克预测模型并进行准确性测试,并根据准确性测试结果选取最优预测 模型;模型使用模块,用于将所述最优预测模型适配于医疗应用端中的临床辅助决策系统, 并在待诊患者符合预设触发条件时,利用所述最优预测模型对所述待诊患者进行诊断,并 输出至少包括儿童血液肿瘤患者脓毒性休克信息的预测结果。 为实现上述目的及其他相关目的,本申请的第三方面提供一种计算机可读存储介 质,其上存储有计算机程序,所述计算机程序被处理器执行时实现所述儿童血液肿瘤患者 脓毒性休克预测方法。 为实现上述目的及其他相关目的,本申请的第四方面提供一种计算机设备,包括: 处理器及存储器;所述存储器用于存储计算机程序,所述处理器用于执行所述存储器存储 的计算机程序,以使所述终端执行所述儿童血液肿瘤患者脓毒性休克预测方法。 如上所述,本申请的儿童血液肿瘤患者脓毒性休克预测方法、装置、终端及介质, 具有以下有益效果:本发明旨在利用医院电子病历信息库,结合机器学习的方法,建立脓毒 性休克的机器学习模型,并将模型嵌入医生工作站的临床辅助决策系统(CDSS),对住院患 儿实施实时监控,早期识别脓毒性休克高危患儿,以给予临床医生更多的临床诊疗支持。因 此本发明将模型部署到临床场景中进行实际应用,以帮助医生预测儿童血液肿瘤患者的脓 毒性休克风险,降低儿童血液肿瘤住院患者在粒缺发热期的脓毒性休克发生率。在回顾性 资料中被临床医生评估为对临床有帮助价值,具体体现为可提前预测85%的脓毒性休克患 儿,降低致死和致残率。 附图说明 图1显示为本申请一实施例中儿童血液肿瘤患者脓毒性休克预测方法的流程示意 5 CN 111599466 A 说 明 书 3/9 页 图。 图2显示为本申请一实施例中儿童血液肿瘤患者脓毒性休克预测模型构建流程示 意图。 图3显示为本申请一实施例中儿童血液肿瘤患者脓毒性休克预测模型输出结果示 意图。 图4显示为本申请一实施例中儿童血液肿瘤患者脓毒性休克预测装置的结构示意 图。 图5显示为本申请一实施例中计算机设备的结构示意图。
技术实现要素:
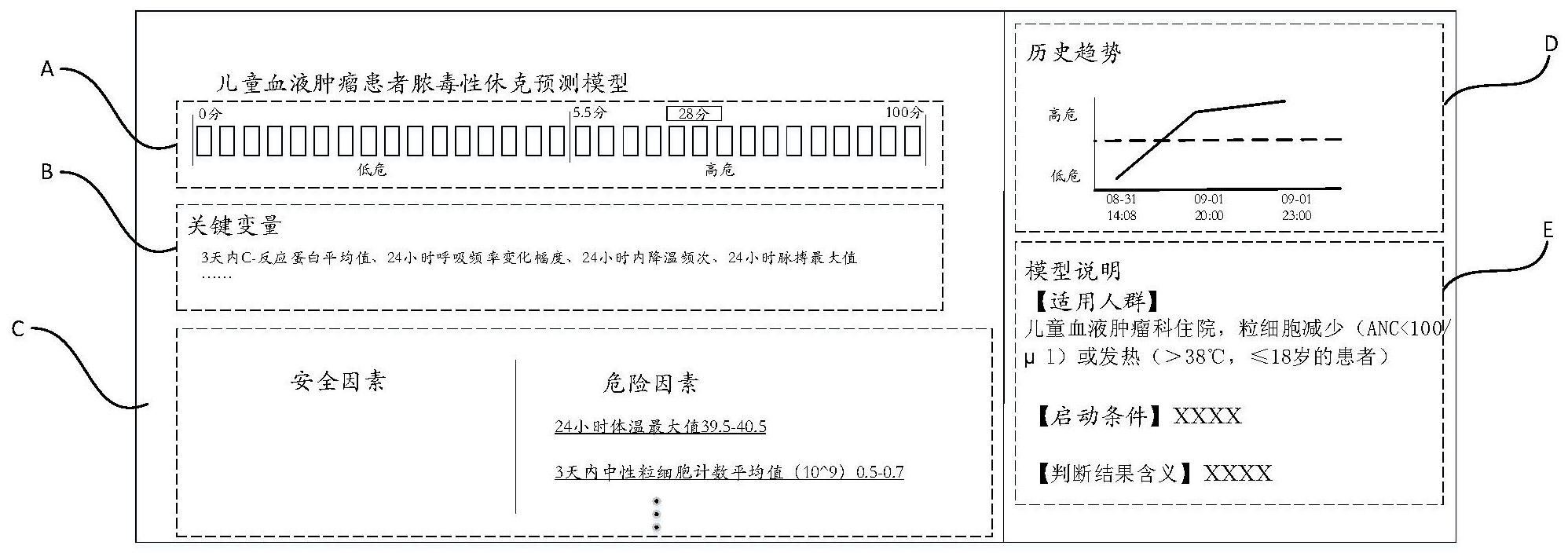
以下通过特定的具体实例说明本申请的实施方式,本领域技术人员可由本说明书 所揭露的内容轻易地了解本申请的其他优点与功效。本申请还可以通过另外不同的具体实 施方式加以实施或应用,本说明书中的各项细节也可以基于不同观点与应用,在没有背离 本申请的精神下进行各种修饰或改变。需说明的是,在不冲突的情况下,以下实施例及实施 例中的特征可以相互组合。 需要说明的是,在下述描述中,参考附图,附图描述了本申请的若干实施例。应当 理解,还可使用其他实施例,并且可以在不背离本申请的精神和范围的情况下进行机械组 成、结构、电气以及操作上的改变。下面的详细描述不应该被认为是限制性的,并且本申请 的实施例的范围仅由公布的专利的权利要求书所限定。这里使用的术语仅是为了描述特定 实施例,而并非旨在限制本申请。空间相关的术语,例如“上”、“下”、“左”、“右”、“下面”、“下 方”、“下部”、“上方”、“上部”等,可在文中使用以便于说明图中所示的一个元件或特征与另 一元件或特征的关系。 在本申请中,除非另有明确的规定和限定,术语“安装”、“相连”、“连接”、“固定”、 “固持”等术语应做广义理解,例如,可以是固定连接,也可以是可拆卸连接,或一体地连接; 可以是机械连接,也可以是电连接;可以是直接相连,也可以通过中间媒介间接相连,可以 是两个元件内部的连通。对于本领域的普通技术人员而言,可以根据具体情况理解上述术 语在本申请中的具体含义。 再者,如同在本文中所使用的,单数形式“一”、“一个”和“该”旨在也包括复数形 式,除非上下文中有相反的指示。应当进一步理解,术语“包含”、“包括”表明存在所述的特 征、操作、元件、组件、项目、种类、和/或组,但不排除一个或多个其他特征、操作、元件、组 件、项目、种类、和/或组的存在、出现或添加。此处使用的术语“或”和“和/或”被解释为包括 性的,或意味着任一个或任何组合。因此,“A、B或C”或者“A、B和/或C”意味着“以下任一个: A;B;C;A和B;A和C;B和C;A、B和C”。仅当元件、功能或操作的组合在某些方式下内在地互相 排斥时,才会出现该定义的例外。 本发明旨在利用医院电子病历信息库,结合机器学习的方法,建立脓毒性休克的 机器学习模型,并将模型嵌入医生工作站的临床辅助决策系统(CDSS),对住院患儿实施实 时监控,早期识别脓毒性休克高危患儿,以给予临床医生更多的临床诊疗支持。因此本发明 将模型部署到临床场景中进行实际应用,以帮助医生预测儿童血液肿瘤患者的脓毒性休克 风险,降低儿童血液肿瘤住院患者在粒缺发热期的脓毒性休克发生率。在回顾性资料中被 6 CN 111599466 A 说 明 书 4/9 页 临床医生评估为对临床有帮助价值,具体体现为可提前预测85%的脓毒性休克患儿,降低 致死和致残率。 为了使本发明的目的、技术方案及优点更加清楚明白,通过下述实施例并结合附 图,对本发明实施例中的技术方案的进一步详细说明。应当理解,此处所描述的具体实施例 仅用以解释本发明,并不用于限定发明。 实施例一: 如图1所示,展示了本发明一实施例中儿童血液肿瘤患者脓毒性休克预测方法的 流程示意图,由主要的子步骤S11~S13构成。 需说明的是,本实施例的预测方法可应用于计算机设备,所述计算机设备包括但 不限于如台式电脑、笔记本电脑、平板电脑、智能手机、智能电视、个人数字助理(Personal Digital Assistant,简称PDA)等个人电脑。在另一些实施方式中,所述预测方法也可应用 于服务器,所述服务器可以根据功能、负载等多种因素布置在一个或多个实体服务器上,也 可以由分布的或集中的服务器集群构成,本实施例不作限定。 步骤S11:构建儿童血液肿瘤患者脓毒性休克数据集,据以构建儿童血液肿瘤患者 脓毒性休克预测模型;本步骤的子步骤如图2所示,包括子步骤S111~S113。 步骤S111:根据预设条件选取样本人群并采集源数据。举例来说,可选取某儿童医 学中心在一段时间内血液肿瘤科入院且符合研究纳排规则患者的临床电子病历数据,血液 肿瘤科住院且发生粒减或发热的患者作为建模样本。源数据是驱动决策的基础,数据越全 推荐的内容越完整,本实施例涉及的源数据包括但不限于患者的基本信息数据、药品医嘱 信息数据、检查检验信息数据、手术及处理信息数据、护理及体征数据等。 步骤S112:从所述源数据中抽取病例组和对照组并进行预处理。 具体来说,可通过医学专家回顾性人工标注的方法在标记每个样本的结局标签, 分为住院期发生脓毒性休克的病例组(阳性样本)以及住院期未发生脓毒性休克的对照组 (阴性样本)。随后分别抽取出病例组和对照组的相关资料进行检查、整理、以及数据清洗等 预处理。其中的数据清洗主要是对异常值进行检视修复,对缺失率较高(例如缺失率>50%) 的变量予以删除。应理解的是,所述病例组是指正类样本(y=1),即有相应感染的样本;所 述对照组是指负类样本(y=0),即没有相应感染的样本。 步骤S113,基于预处理后的数据,选取入模特征变量并构建儿童血液肿瘤患者脓 毒性休克预测模型。 具体来说,可运用机器学习算法等方法探究儿童血液肿瘤住院患者的脓毒性休克 危险因素,并结合专家的经验选定模型的入模特征变量,最终建立儿童血液肿瘤粒减/发热 患者的脓毒性休克多临床因素预测模型。为便于本领域技术人员理解,下文将结合表1展示 和儿童血液肿瘤患者脓毒性休克预测相关联的入模特征变量。 表1—入模特征变量 7 CN 111599466 A 说 明 书 5/9 页 在本实施例优选的实现方式中,所述儿童血液肿瘤患者脓毒性休克预测模型包括 但不限于Xgboost模型、Scorecard模型、Neural Network模型、SVM模型、Logistic Regression模型、Decision Tree模型、Random Forest模型等等。 在本实施例可选的实现方式中,由于入模特征变量往往有很多个值,例如某患者 的体温特征,在入院时需要测量体温而且之后每日都需要测量一次体温,因此无法给预测 模型输入稳定的变量,而且也无法体现单个参数变量内不同值之间的关系。有鉴于此,本实 施例的技术方案基于时间窗对入模特征变量进行聚合衍生处理,以达到给预测模型输入稳 定的变量的目的,也能体现单个入模特征变量中不同值之间的关联关系,例如不同值之间 的变换、趋势、分布等情况。 首先确定时间窗,例如可根据医学逻辑为每个入模特征变量指定时间窗来确定取 值的时间范围,例如8小时内、16小时内、1天内、2天内、3天内、1周内、1个月内、1年内,甚或 全历史等等,本实施例不作限定。 其次在确定时间窗后,部分甚至全部的入模特征变量往往会取到多个不同的值, 因此将这些不同的值进行聚合,从而体现出这些值之间的变换、趋势、分布等关系,最终基 于医学逻辑及模型效果,给相应入模特征变量配上最适合的聚合方式,固化并进入模型。 本实施例涉及的聚合衍生处理包括但不限于如下方式: 1)有无预测:有则为1,否则为0; 2)计数:计算所有被标记为出现的次数; 3)取最大值:取系列中最大的一个值; 4)取最小值:取系列中最小的一个值; 5)取平均值:取系列中的算术平均值; 6)取最末值:取系列中对应绝对时间最大的一个值; 7)取最早值:取系列中对应绝对时间最小的一个值; 8 CN 111599466 A 说 明 书 6/9 页 8)取平均发展速度值:用于衡量该特征变量在指定时间窗内的整体平局增长速 度; 9)取标准差值:用于衡量该特征变量在指定时间窗内的整体平局增长速度; 10)取最大增幅值:用于衡量该特征变量在指定时间窗内的的最大变化幅度。 步骤S12:训练所述儿童血液肿瘤患者脓毒性休克预测模型并进行准确性测试,并 根据准确性测试结果选取最优预测模型。 具体来说,由于机器学习算法有多种,因此本发明在机器学习系统中会对多种机 器学习算法进行批量的实验,并完成超参数自动化搜索,对每个模型进行逐轮的算法准确 性测试,从中选择准确性最优的模型使用。举例来说,可在机器学习中对Xgboost模型、 Scorecard模型、Neural Network模型、SVM模型、Logistic Regression模型、Decision Tree模型、Random Forest模型等进行批量的实验,对每个模型进行算法准确性测试,最终 选择准确性最高的Xgboost模型使用。 在本实施例可选的实现方式中,对每个模型的准确性评价采用AUC(Area Under Curve),即ROC曲线下的面积,取值通常接于0.1~1之间,AUC值可直观地评价分类器的好 坏,值越大越好。AUC的计算公式如下式1)所示: 其中,M表示正类样本的数量;N为负类样本的数量;n表示样本总数(M N)。AUC值的 计算原理如下:首先是对所有样本的得分(score)从大到小进行排序,然后令得分最大的样 本的排序(rank)为n,并令得分第二大的样本的排序(rank)为n-1,以此类推;其次是把所有 的正类样本的排序相加,再减去(M-1)种两个样本组合的情况,得到的就是所有样本中有多 少对正类样本的得分大于负类样本的得分,然后再除以(M×N)。 步骤S13:将所述最优预测模型适配于医疗应用端中的临床辅助决策系统,并在待 诊患者符合预设触发条件时,利用所述最优预测模型对所述待诊患者进行诊断,并输出至 少包括儿童血液肿瘤患者脓毒性休克信息的预测结果。 具体来说,可将最优预测模型开发成软件接口,并和医疗服务器中的临床辅助决 策系统(CDSS)对接,当患者信息符合临床辅助决策系统(CDSS)设置的预设触发条件时,对 这名患者进行AI模型诊断,即利用最优预测模型来进行诊断,并通过通讯工具将AI模型输 出的风险结果及相关说明传送给相关的终端医生。 在本实施例可选的实现方式中,所述预设触发条件包括:儿童血液肿瘤科住院,年 龄≤18岁的患者,且粒细胞减少(ANC<1000/μl)或发热(体温>38℃)。上述患者入院8小时 后并可获得必须变量内容时启动,持续运行直至达到退出条件。前述的退出条件包括:患者 出院,或者患者粒细胞恢复(ANC≥1000/μl)且热平(体温≤38℃),并且恢复持续72小时不 再发生粒细胞减少或发热。 在本实施例可选的实现方式中,最优预测模型输出的预测结果包括但不限于:儿 童血液肿瘤患者脓毒性休克的预测信息(如得分和危险级别等)、关键变量、保护因素和危 险因素、一时间段内预测信息的趋势、模型说明(如适用人群、模型启动条件、必需变量、预 测结果含义的解释、阈值含义等等)。为便于本领域技术人员理解,现结合图3来对本发明提 9 CN 111599466 A 说 明 书 7/9 页 供的AI模型的输出结果进行图示解释。 图3的区域A展示了儿童血液肿瘤患者脓毒性休克预测模型的预测结果信息,从左 到右得分跨越区间0~100分,分值越高危险等级越高,本实施例中患者的预测分值为28分; 而且随着危险等级的变化,分值区域的颜色也可相应发生变化,例如低危区域采用感观上 较为安全的绿色,中危区域采用感观上相对安全的黄色,高危区域则采用感观上较为危险 的红色,更便于医生用户分辨。 图3的区域B展示了关键变量,例如3天内C-反应蛋白平均值、24小时呼吸频率变化 幅度、24小时内降温频次、24小时脉搏最大值等等。 图3的区域C展示了保护因素和危险因素,例如危险因素有24小时体温最大值 39.5-40.5,3天内中性粒细胞计数平均值(10^9)0.5-0.7等等。 图3的区域D展示了一时间段内预测信息的趋势,例如患者从08月31日到09月01日 这一时间段内预测结果从低危变为高危而且仍呈上升趋势。 图3的区域E展示了模型说明,例如对适用人群进行的说明“儿童血液肿瘤科住院, 粒细胞减少(ANC<100/μl)或发热(>38℃,≤18岁的患者)”,对模型启动条件的说明,对预 测结果含义的解释等,本实施例不做限定。 本领域技术人员应理解的是,以上实施例中AI模型输出界面中的各展示区域的排 布,以及各展示区域内的内容,都只作为示例而非用于限定本发明的范围。 总结来说,本实施例提供的预测模型在回顾性资料中被临床医生评估为对临床有 帮助价值,体现为可提前预测85%的脓毒性休克患儿,降低致死和致残率。将模型部署到临 床场景中进行实际应用,以帮助医生预测儿童血液肿瘤患者的脓毒性休克风险,降低儿童 血液肿瘤住院患者在粒缺发热期的脓毒性休克发生率。 本发明提供的预测模型已在临床应用场景中做过大量的测试,下文就其中一组测 试来说明本发明的预测模型的有效性:对测试集中的310个就诊(2019年1月后的入院)均模 拟了入院后每个小时的时序曲线,通过AI评估结果对比当时的历史病程记录,选择预测结 果分值>11.4分(0.114)作为高危阈值,在测试数据集中则可以将85%的脓毒性休克病例 在脓毒性休克前48小时内进行高危提示。 1、AI可以早于脓毒性休克提前预警85%的患者; 2、当时的临床医生未提高警觉,若AI能进行提醒,则可能提升临床关注程度,改变 患者结局,减少因此病而导致的致死和致残。 实施例二: 如图4所示,展示了本发明一实施例中的儿童血液肿瘤患者脓毒性休克预测装置 的结构示意图。本实施例中的预测装置包括模型构建模块41、模型测试模块42和模型使用 模块43。 具体而言,模型构建模块41用于构建儿童血液肿瘤患者脓毒性休克数据集,据以 构建儿童血液肿瘤患者脓毒性休克预测模型。模型测试模块42用于训练所述儿童血液肿瘤 患者脓毒性休克预测模型并进行准确性测试,并根据准确性测试结果选取最优预测模型。 模型使用模块43用于将所述最优预测模型适配于医疗应用端中的临床辅助决策系统,并在 待诊患者符合预设触发条件时,利用所述最优预测模型对所述待诊患者进行诊断,并输出 至少包括儿童血液肿瘤患者脓毒性休克信息的预测结果。 10 CN 111599466 A 说 明 书 8/9 页 需要说明的是,本实施例提供的装置和上文中的方法的实施方式类似,故不再赘 述。另外需要说明的是,应理解以上装置的各个模块的划分仅仅是一种逻辑功能的划分,实 际实现时可以全部或部分集成到一个物理实体上,也可以物理上分开。且这些模块可以全 部以软件通过处理元件调用的形式实现;也可以全部以硬件的形式实现;还可以部分模块 通过处理元件调用软件的形式实现,部分模块通过硬件的形式实现。例如,模型构建模块可 以为单独设立的处理元件,也可以集成在上述装置的某一个芯片中实现,此外,也可以以程 序代码的形式存储于上述装置的存储器中,由上述装置的某一个处理元件调用并执行以上 模型构建模块的功能。其它模块的实现与之类似。此外这些模块全部或部分可以集成在一 起,也可以独立实现。这里所述的处理元件可以是一种集成电路,具有信号的处理能力。在 实现过程中,上述方法的各步骤或以上各个模块可以通过处理器元件中的硬件的集成逻辑 电路或者软件形式的指令完成。 例如,以上这些模块可以是被配置成实施以上方法的一个或多个集成电路,例如: 一个或多个特定集成电路(Application Specific Integrated Circuit,简称ASIC),或, 一个或多个微处理器(digital signal processor,简称DSP),或,一个或者多个现场可编 程门阵列(Field Programmable Gate Array,简称FPGA)等。再如,当以上某个模块通过处 理元件调度程序代码的形式实现时,该处理元件可以是通用处理器,例如中央处理器 (Central Processing Unit,简称CPU)或其它可以调用程序代码的处理器。再如,这些模块 可以集成在一起,以片上系统(system-on-a-chip,简称SOC)的形式实现。 实施例三: 如图5所示,展示了本申请实施例提供的再一种计算机设备的结构示意图。本实例 提供的计算机设备,包括:处理器51、存储器52、通信器53;存储器52通过系统总线与处理器 51和通信器53连接并完成相互间的通信,存储器52用于存储计算机程序,通信器53用于和 其他设备进行通信,处理器51用于运行计算机程序,使计算机设备执行如上儿童血液肿瘤 患者脓毒性休克预测方法的各个步骤。 上述提到的系统总线可以是外设部件互连标准(Peripheral Component Interconnect,简称PCI)总线或扩展工业标准结构(Extended Industry Standard Architecture,简称EISA)总线等。该系统总线可以分为地址总线、数据总线、控制总线等。 为便于表示,图中仅用一条粗线表示,但并不表示仅有一根总线或一种类型的总线。通信接 口用于实现数据库访问装置与其他设备(例如客户端、读写库和只读库)之间的通信。存储 器可能包含随机存取存储器(Random Access Memory,简称RAM),也可能还包括非易失性存 储器(non-volatile memory),例如至少一个磁盘存储器。 上述的处理器可以是通用处理器,包括中央处理器(Central Processing Unit, 简称CPU)、网络处理器(Network Processor,简称NP)等;还可以是数字信号处理器 (Digital Signal Processing,简称DSP)、专用集成电路(Application Specific Integrated Circuit,简称ASIC)、现场可编程门阵列(Field-Programmable Gate Array, 简称FPGA)或者其他可编程逻辑器件、分立门或者晶体管逻辑器件、分立硬件组件。 实施例四: 本实施例提供一种计算机可读存储介质,其上存储有计算机程序,所述计算机程 序被处理器执行时实现所述儿童血液肿瘤患者脓毒性休克预测方法。 11 CN 111599466 A 说 明 书 9/9 页 本领域普通技术人员可以理解:实现上述各方法实施例的全部或部分步骤可以通 过计算机程序相关的硬件来完成。前述的计算机程序可以存储于一计算机可读存储介质 中。该程序在执行时,执行包括上述各方法实施例的步骤;而前述的存储介质包括:ROM、 RAM、磁碟或者光盘等各种可以存储程序代码的介质。 综上所述,本申请提供儿童血液肿瘤患者脓毒性休克预测方法、装置、终端及介 质,旨在利用医院电子病历信息库,结合机器学习的方法,建立脓毒性休克的机器学习模 型,并将模型嵌入医生工作站的临床辅助决策系统(CDSS),对住院患儿实施实时监控,早期 识别脓毒性休克高危患儿,以给予临床医生更多的临床诊疗支持。因此本发明将模型部署 到临床场景中进行实际应用,以帮助医生预测儿童血液肿瘤患者的脓毒性休克风险,降低 儿童血液肿瘤住院患者在粒缺发热期的脓毒性休克发生率。在回顾性资料中被临床医生评 估为对临床有帮助价值,具体体现为可提前预测85%的脓毒性休克患儿,降低致死和致残 率。所以,本申请有效克服了现有技术中的种种缺点而具高度产业利用价值。 上述实施例仅例示性说明本申请的原理及其功效,而非用于限制本申请。任何熟 悉此技术的人士皆可在不违背本申请的精神及范畴下,对上述实施例进行修饰或改变。因 此,举凡所属技术领域中具有通常知识者在未脱离本申请所揭示的精神与技术思想下所完 成的一切等效修饰或改变,仍应由本申请的权利要求所涵盖。 12 CN 111599466 A 说 明 书 附 图 1/3 页 图1 图2 13 CN 111599466 A 说 明 书 附 图 2/3 页 图3 图4 14 CN 111599466 A 说 明 书 附 图 3/3 页 图5 15












