技术摘要:
本发明涉及来源于土曲霉菌Aspergillus terreus NIH2624转氨酶(XP_001209325.1)突变体多肽、编码所述多肽的多核苷酸以及使用所述多肽在(R)‑1‑BOC‑3‑氨基哌啶制备上的应用。本发明通过计算机模拟对转氨酶定向改造,改造氨基酸位点选自Y60、V62、F115、W184、G216、F2 全部
背景技术:
: 糖尿病主要是由于机体胰岛素分泌不足或胰岛素作用障碍引起的以高血糖为特 征的代谢疾病。其中胰岛素分泌不足被定义为Ⅰ型、胰岛素作用障碍被定义为Ⅱ型糖尿病, Ⅱ型糖尿病患者占糖尿病患者的90%以上。 目前治疗Ⅱ型糖尿病的药物主要分为磺酰脲类、双胍类、α-葡萄糖苷酶抑制剂、胰 岛素增敏剂、噻唑烷二酮类、二肽基肽酶IV(DPP-IV)抑制剂等几大类,其中目前公认最为高 效安全的是(DPP-IV)抑制剂,该类药物能够选择性与二肽基肽酶IV可逆性结合从而抑制二 肽基肽酶IV的活性,进而延缓胰高血糖素样肽-1(GLP-1)和抑胃肽(GIP)降解,从而调节糖 尿病Ⅱ型患者的血糖水平。 市 售 二 肽 基 肽 酶 I V ( D P P - I V ) 抑 制 剂 主 要 有 西 他 列 汀 (Sitagliptinintermediate)、曲格列汀琥珀酸盐(Trelagioptinsuccimate)、利拉利汀 (Linagliptin)、苯甲酸阿格列汀(Alogliptiubenxoute),而在这些二肽基肽酶IV(DPP-IV) 抑制剂的合成中(R)-N-Boc-3-氨基哌啶扮演着非常重要的角色。例如由德国勃林格殷格翰 公司公布的利拉利汀(Linagliptin)技术路线中(R)-N-Boc-3-氨基哌啶直接参与利拉利汀 (Linagliptin)核心骨架的形成。 目前(R)-N-Boc-3-氨基哌啶的合成方法主要以不对称合成,CN103588699中以N- Boc-3-哌啶酮为原料,使用(R)-α-甲基苄胺作为手性辅助基团与其反应得到中间体烯胺, 再将烯胺通过手性辅助基团的控制加氢还原,得到最终脱去手性辅助基团后的N-Boc-(R)- 3-氨基哌啶。无独有偶,CN105111134中以N-Boc-3-哌啶酮为原料,使用叔丁基亚磺酰胺作 为手性辅助基团与其反应得到亚磺酰亚胺,同样采用手性辅助基团的控制加氢还原的方 式,最终同样得到了N-Boc-(R)-3-氨基哌啶。但是不对称合成需进行拆分或通过重结晶方 式提高中间体或产物的光学纯度,存在反应步骤较多,收率较低的问题。 PCT专利申请公布文本WO2005000305中,以3-羟基哌啶为原料,经上保护、甲磺酸 酯化、叠氮化、还原反应最终得到N-Boc-(R)-3-氨基哌啶,但是其本身原料价格较高,同时 叠氮化反应中的叠氮化钠相对来说比较危险,这一特性严重影响了其工业化推进的可能。 PCT专利申请公布文本WO2007075630中,以2,5二氨基戊酸为原料,与甲醇发生酯 化,进而反应成环、还原反应、加上保护基团,同样得到了N-Boc-(R)-3-氨基哌啶。但是该合 成路线中直接以手性原料为起始,在后续成互不成环反应中容易消旋化,影响产物的光学 纯度。并且增加保护基团这一过程条件相对严苛,否则会出现3位氨基也被保护的可能。
技术实现要素:
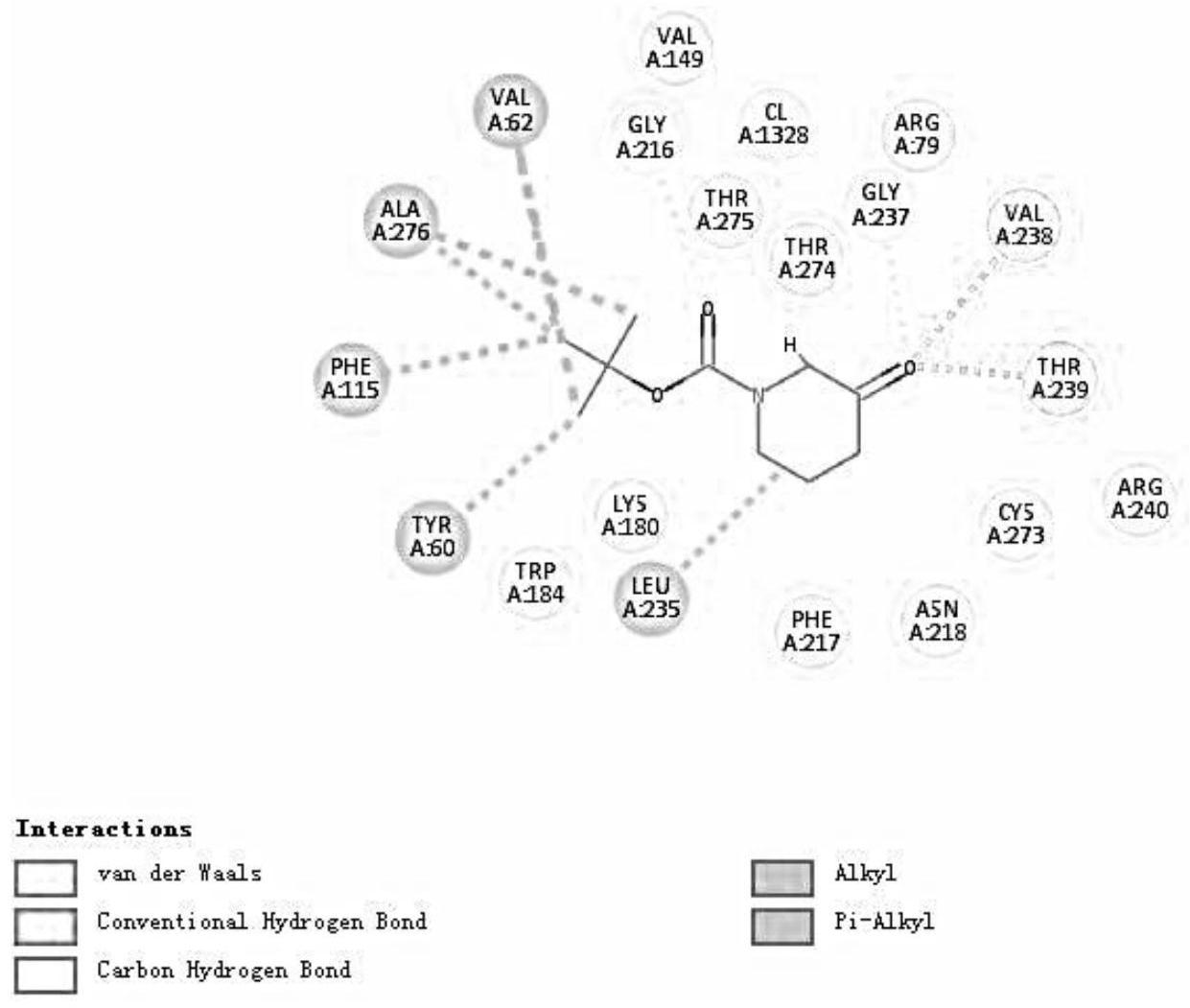
: 为解决上述问题,本发明以来源于土曲霉菌Aspergillus terreus NIH2624的转 3 CN 111549011 A 说 明 书 2/10 页 氨酶基因XP_001209325.1为研究对象,通过计算机模拟对XP_001209325.1理性预测并进行 定点突变,以提高转氨酶的选择性及活性。 本发明的主要目的是提高来源于土曲霉菌Aspergillus terreus NIH2624的转氨 酶对非天然底物N-BOC-3-派啶酮催化活力,得到酶活显著提高的转氨酶突变体,解决现有 (R)-1-BOC-3-氨基哌啶合成技术中存在的缺陷。 本发明的技术方案如下: 步骤1:候选转氨酶与反应底物N-BOC-3-派啶酮的分子对接评估。 步骤2:针对分子对接结果优选评估分数较高的转氨酶进行活性测试。 步骤3:选择催化活性与立体选择性最高的Aspergillus terreus NIH2624的转氨 酶作为本发明的野生型转氨酶。 步骤4:虚拟突变Aspergillus terreus NIH2624转氨酶活性中心周围单个氨基酸 确定氨基酸突变位点。 步骤5:Aspergillus terreus NIH2624转氨酶活性中心氨基酸区域单突变活性及 选择性测试。 步骤6:Aspergillus terreus NIH2624转氨酶活性中心氨基酸区域组合突变体活 性测试。 步骤7:N-BOC-3-派啶酮的催化条件优化。 1.本发明根据虚拟氨基酸位点单突变结果,重点突变了V62W/K/P、N218R、L235K/ R、G237K/R、V238R/K、T239K/R、T275K的组合。 2 .本发明所述的分区域,指将15个单突变位点分为Ⅰ区(60、62位氨基酸)、Ⅱ区 (115位氨基酸)、Ⅲ区(184位氨基酸)、Ⅳ区(216、217、218位氨基酸)、Ⅴ区(235、237、238、 239位氨基酸)、Ⅵ区(273、274、275、276位氨基酸)。 3.本发明所述的区域组合,指将6个区域进行2-6个区域中1-6个突变位点组合得 到转氨酶组合突变体。 4.本发明还提供了所述转氨酶突变体的编码多核苷酸序列。 5.本发明还提供了所述转氨酶突变体的编码多核苷酸序列的表达载体与工程菌。 6.本发明还提供了所述转氨酶突变体在催化N-BOC-3-派啶酮制备(R)-1-BOC-3- 氨基哌啶的应用。 7.本发明还提供了一种催化N-BOC-3-派啶酮制备(R)-1-BOC-3-氨基哌啶的方法, 步骤包括: (1)制备表达转氨酶突变体的基因工程菌,所述转氨酶突变体如上述1和2所述; (2)培养所述基因工程菌,制备酶液; 步骤(2)中,所述的酶液最优为粗酶液进行纯化获得的纯酶,当然基因工程菌的静 息细胞悬液或者破胞粗酶液也适用本发明所述的(R)-1-BOC-3-氨基哌啶制备方法。 (3)将所述酶液加入含有底物N-BOC-3-派啶酮、异丙氨及PLP的混合体系中,进行 转氨反应,制得(R)-1-BOC-3-氨基哌啶。 在上述(R)-1-BOC-3-氨基哌啶的酶催化制备方法中,作为优选,所述酶催化反应 的温度为40℃~44℃,该温度区间内具有反应条件温和转化率高的优点。 在上述(R)-1-BOC-3-氨基哌啶的酶催化制备方法中,作为优选,所述酶催化反应 4 CN 111549011 A 说 明 书 3/10 页 在pH值为8.0~10.0。该pH区间能更有效的保证酶的活性,提高酶催化反应的效果。 在上述(R)-1-BOC-3-氨基哌啶的酶催化制备方法中,作为优选,所述酶催化反应 还在磷酸盐缓冲液或Tris-HCl缓冲液中进行。通过该缓冲液的存在,能够反应体系处于一 定较平稳的pH值体系,避免体系中的pH值变化过大,更有效的保证反应的稳定进行。 在上述(R)-1-BOC-3-氨基哌啶的酶催化制备方法中,作为优选,所述酶催化反应 在最适合酶用量为2~80mg/g。 综上所述,本发明与现有技术相比,具有以下优点: 通过采用本发明的具有如权利要求1和2所示的氨基酸序列的相应转氨酶,在相应 的催化体系下,能够有效的使底物N-BOC-3-派啶酮转化成高手性的产物(R)-1-BOC-3-氨基 哌啶,且具有收率高的优点,解决现有(R)-1-BOC-3-氨基哌啶合成技术中存在的缺陷。 说明书附图: 图1:N-BOC-3-派啶酮与Aspergillus terreus NIH2624转氨酶相互作用图; 图2:N-BOC-3-派啶酮与Aspergillus terreus NIH2624转氨酶相互作用图二维平 面图。












