技术摘要:
本发明提供了一种提高或改善普拉克索及其药用盐制剂稳定性的方法,并进而提供一种盐酸普拉克索水溶液形式的口服给药的药物组合物。本发明的口服溶液,制备工艺简单,化学稳定性好,可解决多剂量给药问题,进一步避免老年患者的吞咽问题,本发明的口服溶液与含有盐酸普 全部
背景技术:
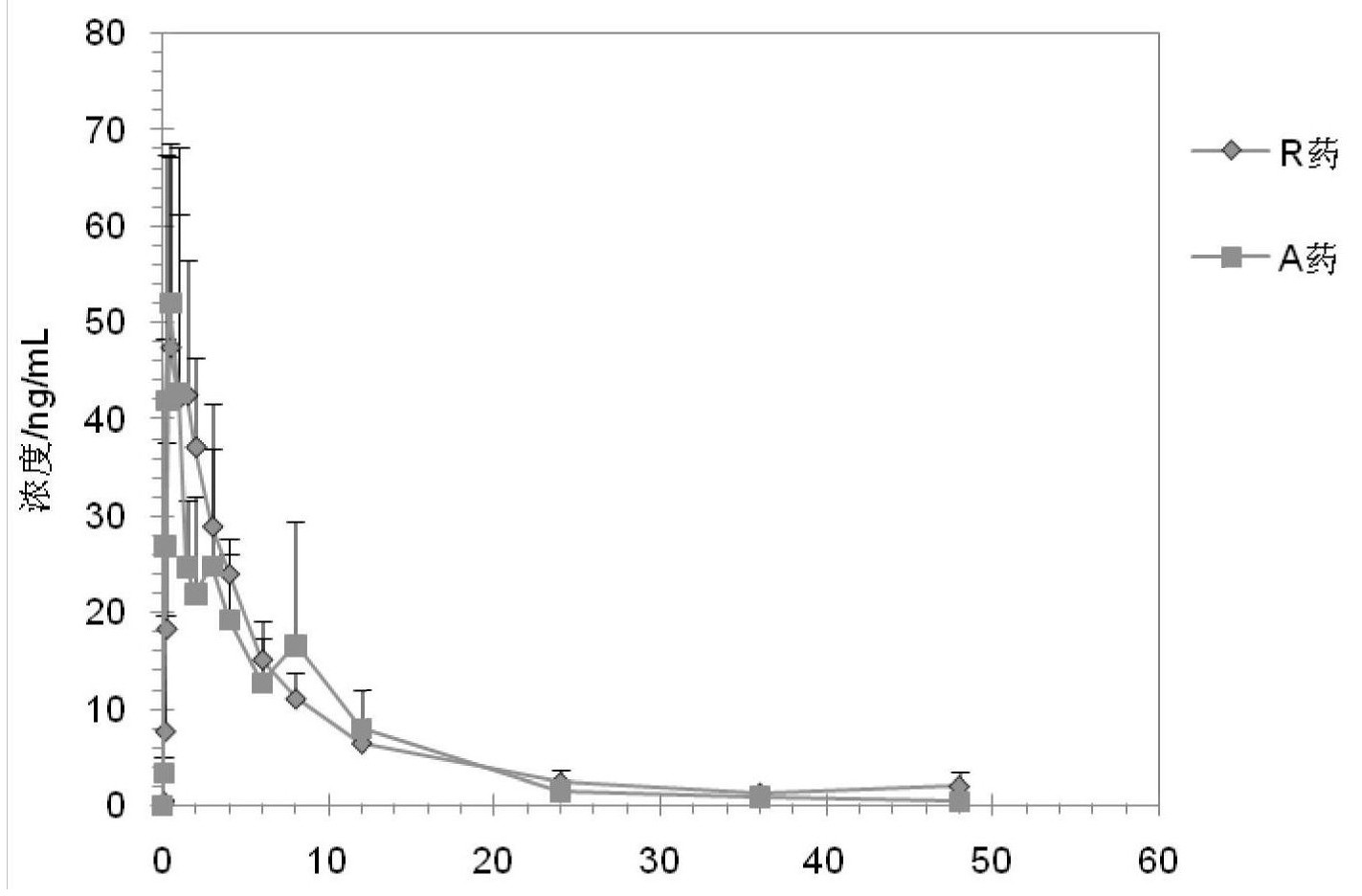
为解决普拉克索或其药用盐制剂,特别是溶液剂型存在的存放不稳定问题,发明 人在研究中令人意外地发现了提高或改善普拉克索或其药用盐制剂稳定性的方法,并进而 提供一种存放稳定的普拉克索或其盐的制剂,尤其是提供了一种新的盐酸普拉克索口服溶 液。 本发明技术方案如下: 本发明提供一种提高或改善普拉克索或其药用盐制剂稳定性的方法,其特征在于 所述制剂中不含缓冲剂和/或缓冲剂系统。 优选地,上述所述的方法,其中所述普拉克索或其药用盐为盐酸普拉克索。 本发明上述所述的方法,其中所述的制剂,优选为溶液剂型,例如为口服溶液或注 3 CN 111588692 A 说 明 书 2/9 页 射溶液;更优选地,所述的制剂为口服液。 作为本发明另一目的,还提供了一种盐酸普拉克索口服液,其包含盐酸普拉克索、 防腐剂和水,其特征在于所述口服液不含缓冲剂或缓冲剂系统。 优选地,上述所述的盐酸普拉克索口服液,其中所述的防腐剂可以为尼泊金酯或 其盐、苯甲酸或其盐类、山梨酸或其盐类。 更优选地,上述所述的盐酸普拉克索口服液,其中所述的防腐剂选自尼泊金甲酯、 尼泊金丙酯、尼泊金乙酯、尼泊金丁酯、尼泊金甲酯钠、尼泊金乙酯钠、尼泊金丙酯钠、尼泊 金丁酯钠、苯甲酸、苯甲酸钠、山梨酸、山梨酸钾中的一种或多种;更优选地,所述的防腐剂 为尼泊金甲酯和/或尼泊金丙酯。 优选地,上述所述的盐酸普拉克索口服液,其特征在于还含有螯合剂;优选地,所 述的螯合剂选自氨基三乙酸、羟乙基乙二胺三乙酸、二亚乙基三胺五乙酸、乙二胺四乙酸、 乙二胺四乙酸二钠(EDTA-2Na)、乙二胺四乙酸钙钠(EDTA-CaNa2)中的一种或多种。 如果需要,本发明上述所述的盐酸普拉克索口服溶液,还可以含有矫味剂,该矫味 剂通常指甜味剂或香味剂。 甜味剂可选自蔗糖、木糖醇、山梨醇、果糖、葡萄糖、阿司帕坦、三氯蔗糖、安赛蜜、 糖精钠中的一种或多种,例如优选为三氯蔗糖。 香味剂通常指水果味香精,可选自草莓香精、橙味香精、荔枝香精、混合莓味香精、 香蕉香精、桔味香精、葡萄香精、青柠香精等的一种或两种,例如优选为混合莓味香精。 本发明上述所述的盐酸普拉克索口服液,其中,每单位制剂中,盐酸普拉克索含量 为0.01mg/ml~10mg/ml;优选地,每单位制剂中盐酸普拉克索含量为0.02mg/ml~1.0mg/ ml;优选地,每单位制剂中盐酸普拉克索含量为0.05mg/ml~0.3mg/ml;作为本发明的具体 实施方式,本发明上述所述的盐酸普拉克索口服液,更优选地,每单位制剂或每单位剂量 中,盐酸普拉克索含量为0.125~0.25mg/ml。 本发明的普拉克索或其盐制剂,特别是盐酸普拉克索口服溶液剂,不含缓冲剂和/ 或缓冲剂系统,制剂显示出优良的稳定性和生物利用度。缓冲剂,也被称为酸碱稳定剂,一 般是盐类,如强酸弱碱或弱酸强碱盐类,在反应或保存中逐渐释出盐中的酸或碱以保持稳 定的酸碱值;缓冲剂系统一般是弱酸或弱碱与其盐的混合物。本发明所述的缓冲剂或缓冲 剂系统,是指制药领域中常用的或常规的缓冲剂或缓冲剂系统,没有特别限制,例如,包括 但不限于枸橼酸-磷酸氢二钠缓冲溶液、枸橼酸-枸橼酸钠缓冲溶液、磷酸二氢钠-氢氧化钠 缓冲溶液、酒石酸-氢氧化钠、磷酸盐缓冲液等。 本发明上述所述的盐酸普拉克索口服液,其中防腐剂、螯合剂、矫味剂的含量或用 量,可以根据需要,按本领域中常规的用量,没有特别的限制。例如,所述的盐酸普拉克索口 服液,每单位制剂或每单位剂量中,防腐剂含量通常为0.02%~0.5%(w/v);螯合剂通常含 量为0.01-0.25%(w/v),矫味剂含量为0.01-60%(w/v)。优选的,防腐剂含量可以为0.02% ~0.2%(w/v),螯合剂含量可以为0.01~0.05%(w/v),矫味剂含量可以为0.1-10%(w/v)。 本发明令人惊讶地发现,普拉克索或其药用盐制剂,特别是盐酸普拉克索口服溶 液剂,在不含缓冲剂和/或缓冲剂系统时,制剂的稳定性具有显著提高或改善,将盐酸普拉 克索与防腐剂和水混合在一起形成的溶液制剂显示出优良的稳定性和生物利用度,取得令 人预料不到的效果,从而提供一种简单、稳定的盐酸普拉克索口服液,且因其可完美的实现 4 CN 111588692 A 说 明 书 3/9 页 多剂量给药问题,为临床提供了一种新型的盐酸普拉克索的给药方案,可有效地治疗帕金 森症以改善患者用药的顺应性及可及性。 附图说明 图1:本发明实施例2的口服制剂与比较制剂盐酸普拉克索片(规格:0.25mg)的生 物利用度对比结果图 其中:R药-指比较制剂;A药-指实施例2的制剂。
技术实现要素:
通过下面的实施例可以对本发明进行进一步描述,但本发明的范围并不限于下述 实施例。 在下面配置各种组合物中,如未另外说明,每批的总配液量为10000ml,但是列明 配方和配置过程时,以每100ml药液中的组成阐明配方和制法,在分装时,每瓶的药液量初 定为100ml。 本发明涉及的检测方法:有关物质检测方法照高效液相色谱法(中国药典2015版 第四部通则0512)测定。 色谱条件和系统适用性试验:用十八烷基硅烷键合硅胶为填充剂(150mm×4.6mm, 5μm);以9.1g磷酸二氢钾-5.0g辛烷磺酸酸钠溶液(用磷酸调节pH值至3.0)为流动相A相,乙 腈-流动相A相(1:1)为流动相B相,乙腈-流动相A相(1:4)为溶剂,检测波长为264nm,流速为 1.5ml/min,进样量为5μl,柱温40±5℃,梯度洗脱程序见下面表1: 表1梯度洗脱程序 时间(min) 0 15 15.1 20 A相% 60 20 60 60 B相% 40 80 40 40 取盐酸普拉克索对照品、杂质A ((6S)-4,5,6,7-tetrahydro-1,3-benzothiazole-2,6-diamine)适量,精密称定, 加溶剂溶解并稀释成每1ml含盐酸普拉克索7.5μg、含杂质A 3.0μg的溶液,作为系统适用性 溶液。精密量取系统适用性溶液5μL注入液相色谱仪,记录色谱图。杂质A和盐酸普拉克索的 分离度不得小于6.0,盐酸普拉克索拖尾因子不得大于2.0。 测定法取本品适量,加溶剂稀释成每1ml含盐酸普拉克索1.5mg的溶液,作为供试 品溶液;精密量取供试品溶液适量,加溶剂溶解并稀释成每1ml含盐酸普拉克索1.5μg的溶 液,作为自身对照溶液。精密量取供试品溶液与自身对照溶液各5μL,分别注入液相色谱仪, 记录色谱图。按以下公式计算,供试品溶液色谱图中如有色谱峰,各杂质峰面积的和不得大 于自身对照溶液主峰面积的5倍(0.5%)。 杂质含量%=(ru/rs)*(Cs/Cu)*100% ru:供试品溶液中每个杂质的峰面积 rs:自身对照溶液中盐酸普拉克索的峰面积 Cs:自身对照溶液中盐酸普拉克索对照品的浓度(mg/ml) Cu:供试品溶液中盐酸普拉克索的浓度(mg/ml) 5 CN 111588692 A 说 明 书 4/9 页 参考例:盐酸普拉克索片在光照和不同温度下的总杂质含量 样品:取有效期内的盐酸普拉克索片(商品名:森福罗,规格0.25mg)进行实验。采 用上述方法对其有关物质进行检测,其结果如下表2所示: 表2盐酸普拉克索片各条件下总杂质含量(%) 结果表明,盐酸普拉克索片在光照、40℃、60℃条件下放置,均有很大程度降解,在 稳定性方面存在较大问题,这对患者用药安全性上存在很大隐患,这也印证有关盐酸普拉 克索片稳定性方面的现有技术报道。 实施例1:盐酸普拉克索口服溶液剂 处方组成如下: 表3实施例1中盐酸普拉克索口服液的配方表 组分 用量(g) 功能 盐酸普拉克索 0.0125 活性成分 尼泊金甲酯 0.18 防腐剂 尼泊金丙酯 0.02 防腐剂 水 99.7875 溶剂 用上述方法对有关物质进行检测,结果分别见表4-5所示。 表4实施例1盐酸普拉克索口服溶液各条件下pH值变化表 表5实施例1盐酸普拉克索口服溶液各条件下总杂质含量(%) 6 CN 111588692 A 说 明 书 5/9 页 实施例2:盐酸普拉克索口服溶液剂 处方组成如下: 表6实施例2中盐酸普拉克索口服液剂的配方表 组分 用量(g) 功能 盐酸普拉克索 0.0125 活性成分 尼泊金甲酯 0.18 防腐剂 尼泊金丙酯 0.02 防腐剂 EDTA-2Na 0.025 螯合剂 水 99.7625 溶剂 用上述方法对有关物质进行检测,结果分别见表7-8所示。 表7实施例2盐酸普拉克索口服溶液各条件下pH值变化表 表8实施例2盐酸普拉克索口服溶液加速条件下总杂质含量(%) 实施例3:盐酸普拉克索口服溶液剂 处方组成如下: 表9实施例3中盐酸普拉克索口服液剂的配方表 7 CN 111588692 A 说 明 书 6/9 页 用上述方法对有关物质进行检测,结果分别见表10-12所示: 表10实施例3处方1盐酸普拉克索口服溶液总杂质含量(%) 表11实施3处方2盐酸普拉克索口服溶液总杂质含量(%) 表12实施例3处方3盐酸普拉克索口服溶液总杂质含量(%) 表13实施例3处方4盐酸普拉克索口服溶液总杂质含量(%) 8 CN 111588692 A 说 明 书 7/9 页 对比例:盐酸普拉克索口服溶液剂 处方组成如下: 表14对比例中盐酸普拉克索口服液剂的配方表 用上述方法对有关物质进行检测,结果分别见表15-16所示。 表15对比例盐酸普拉克索口服溶液各条件下pH值变化表 9 CN 111588692 A 说 明 书 8/9 页 表16对比例盐酸普拉克索口服溶液各条件下总杂质含量(%) 参考例、实施例1-3以及对比例数据可以看出,本发明的口服制剂稳定性均优于盐 酸普拉克索片剂和含有缓冲剂或缓冲剂体系的普拉克索口服制剂。 实施例4:生物等效性试验 10 CN 111588692 A 说 明 书 9/9 页 使用在实施例2中制备的盐酸普拉克索口服溶液剂(0.125mg/ml)以及作为参比制 剂的0.25mg的盐酸普拉克索片,进行了生物等效性试验。给药于空腹状态的Beagles犬(n= 6)的口腔中,让其进行吞咽。在给药前和给药后0.08h、0.17h、0.25h、0.5h、1h、1.5h、2h、3h、 4h、6h、8h、12h、24h、36h和48h时采取血液样品,并通过HPLC-MS分析了血中药浓度。血中浓 度的发展趋势(C-T均数曲线)如图1所示。药代动力学参数的比例,结果如下表17所示。 表17药代动力学参数的比例表(实施例2的制剂/比较制剂) 从图1和表17的结果可知,本发明的口服溶液剂与比较制剂0.25mg盐酸普拉克索 片显示出生物等效性。 11 CN 111588692 A 说 明 书 附 图 1/1 页 图1 12












