技术摘要:
本发明公开了一种基于3D打印特形功能体的血液基因组DNA提取方法及其应用试剂盒,属于核酸提取分离领域。本发明用裂解液对样本进行裂解处理,用3D打印特形功能体进行核酸的结合、分离与纯化。该方法通过手持或机器持在裂解液、清洗液、洗脱液中快速转移3D打印功能体,无 全部
背景技术:
通过血液进行传播的疾病往往引起重大的传染病,带来全球公共卫生安全问题。 预防此类传染病主要根据三条原理:控制传染源、切断传播途径以及保护易感人群,其中最 有效的预防手段是从通过检测病原尽早发现传染源并切断传播,寻求一种方便、快捷、高通 量、高灵敏度的病原检测方法,是提高检测效率和精确度的关键问题。目前常用的病原检测 方法有:病原学检测、免疫学检测及分子生物学检测。 病原学检测常用的是厚、薄血膜染色镜检法,该方法具有操作简单、价格低廉和可 鉴别病原种属等优点,广泛用于疾病的病原学诊断,是目前最常用的方法之一。但血膜染色 镜检法耗时费力、对镜检人员的要求高、灵敏度低,容易造成漏检病原而引起疾病的持续传 播。免疫层析技术作为病原检测的另一常用方法,具有操作简捷、便于携带、设备要求低的 优点。但该方法的经济成本较高,检测受环境、湿度、样品状态而检测结果差异显著,假阴性 或假阳性率高,检测灵敏度低。 PCR(聚合酶链式反应)技术作为分子生物学检测常用的技术,基于核酸为靶标进 行扩增,相较于病原学检测和免疫学诊断具有灵敏度高、特异性好、检测快速的优点,目前 广泛应用于疾病病原的体外PCR诊断。然而,从血液中提取基因组DNA用于疾病病原的体外 PCR诊断,过程复杂、耗时、通量低等问题已经成为限制分子检测技术应用于临床的瓶颈。 从复杂的生物体样本中提取核酸,酚氯仿抽提和trizol法等液相提取手段,因为 污染重,样本需求量大,逐渐被淘汰。固相分离,尤其是磁力分离,借助磁性纳米颗粒结合核 酸并能在外加磁场中快速移动的性能,可以避免传统核酸分离过程中的繁琐离心操作和诸 多手动操作误差,被认为具有下游高通量和自动化应用的前景。然而,纳米颗粒固有的聚 集、沉降效应难以避免,严重制约了核酸提取的效率及稳定性。磁性纳米颗粒解吸核酸困 难、核酸提取效率低也是共性问题,虽有报道提出将磁性纳米粒子与核酸的复合物直接作 为PCR模板可以避免这个问题,但磁性颗粒对PCR扩增过程具有强抑制作用,洗脱过程不可 避免。而对于非磁力的固相分离技术,如传统柱式提取等,将结合核酸的固相载体从裂解液 体系中分离,仍然需要依赖多步离心或反复移液等繁琐操作,导致劳动密集、通量低。 基于此,开发一种过程简单、高通量、快捷的核酸提取及检测方法是研究的重点。 而限制全过程高通量的控制步骤——核酸提取,如何保证提取质量同时提高通量,达到高 通量、快速、简便的目的是需要解决的首要问题。
技术实现要素:
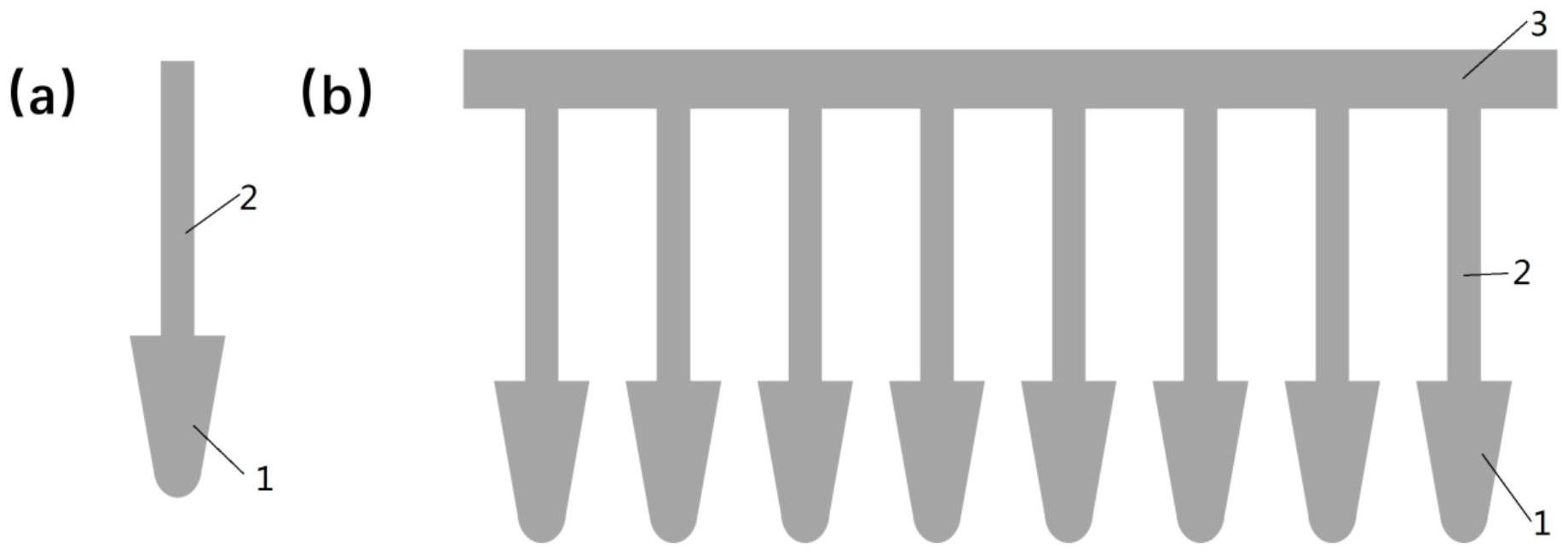
本发明针对目前从血液中提取基因组DNA过程复杂、耗时、通量低等问题,提供了 4 CN 111607635 A 说 明 书 2/7 页 一种基于3D打印特形功能体的血液基因组DNA提取方法。 为解决上述技术问题,本发明所采用的技术方案是:一种基于3D打印特形功能体 的血液基因组DNA提取方法,包括如下步骤: (1)用裂解液对待测血液样本进行裂解处理; (2)通过手持或机器持将3D打印特形功能体的核酸结合区伸入步骤(1)所得溶液 中,进行核酸的结合; (3)通过手持或机器持移动完成步骤(2)的3D打印特形功能体,将核酸结合区伸入 清洗液中,进行核酸清洗; (4)通过手持或机器持将完成步骤(3)的3D打印特形功能体取出,进行干燥; (5)通过手持或机器持将完成步骤(4)的3D打印特形功能体的核酸结合区置入洗 脱液中,进行洗脱,所得洗脱液即为血液基因组DNA。 具体的,上文所述的技术方案中,所述步骤(1)中待测血液样本包括脱离人体或动 物体的血液全血、去掉上清的血红细胞、干血斑。 具体的,上文所述的技术方案中,所述3D打印特形功能体为以光敏树脂或热塑性 塑料为原料,通过3D打印技术获得的具有“伞”型结构的微元件,包括核酸结合区和手柄区。 具体的,上文所述的技术方案中,所述3D打印特形功能体含有1个或至少两个核酸 结合区,为至少两个核酸结合区时,手柄区依靠连接区并排连接在一起;所述核酸结合区为 圆锥体,尺寸为:2-5mm(锥底直径)×5-20mm(高);所述手柄区为圆柱体或长方体,手柄区的 一端与核酸结合区的锥底中心位置连接,构成“伞”型结构;所述核酸结合区表面平整或具 有不平整微观结构,所述不平整微观结构包括螺纹衬托结构、凹槽结构、多孔结构、凸起结 构;所述不平整微观结构可以是任意形状、分布在核酸结合区外表面的任意部位;所述多孔 结构可以是纳米、微米尺寸,多孔结构的形状可以是球体、方体或不规则形状;所述核酸结 合区负载或不负载颗粒材料,所述颗粒材料包括无机盐颗粒和金属颗粒材料,所述无机盐 颗粒包括二氧化硅、二氧化钛、二氧化锰;所述核酸结合区有或者没有官能团修饰,所述官 能团包括羟基、羧基、氨基。所述手柄区的形状为圆柱体或长方体,圆柱体的直径为2-5mm, 长方体的长度为2-5mm,宽度为1-5mm;所述连接区为长方体,尺寸为6.5-10cm(长)×2-10mm (宽)×1-5mm(高)3D打印特形功能体的整体高度h为2.1cm-10cm。 进一步的,利用3D打印技术在打印机上精准制备出特形功能体,核酸结合区、手柄 区、连接区可以是一体制备,也可以是分体制备;当各部分分体制备时,可以通过粘合进行 核酸结合区和手柄区的组装。 具体的,上文所述的技术方案中,所述步骤(1)中裂解液是指能将样本中核酸释放 到溶液中的缓冲液,包括:CTAB裂解液、NaHCO3裂解液、Chelex裂解液、蛋白酶K裂解液或SDS 裂解液。 具体的,上文所述的技术方案中,所述CTAB裂解液包括:1-3%的CTAB、0.5~5M NaCl、0.01~0.05M EDTA、0.05~0.5M Tris-HCl、0.05~0.5%的巯基乙醇,所述NaHCO3裂 解液包括:0.05-1 .00M的NaHCO3、0.5~10%SDS,所述Chelex裂解液包括:0.5~20%的 Chelex-100和0.2~5M的DTT,所述蛋白酶K裂解液包括:20~500mmol的Tris-HCl、10~ 50mmol的EDTA、100~1000mmol的NaCl,0.1~10%的SDS,和5~30μg/mL的蛋白酶K;所述SDS 裂解液包括如下组分:1~20%SDS,0-30μg/mL的蛋白酶K。 5 CN 111607635 A 说 明 书 3/7 页 具体的,上文所述的技术方案中,所述裂解液中加入或不加入RNA消化酶。所述裂 解过程的处理时间为1min-24h,处理温度为0-100℃。 上文所述的技术方案中,所述步骤(2)中进行核酸的结合,具体为将3D打印的特形 功能体的核酸结合区伸入步骤(1)得到的裂解液中,加入或不加入辅助结合溶剂并通过摇 动3D打印特形功能体搅动裂解液的操作,所述辅助结合溶剂可以为异丙醇、无水乙醇中的 一种或两者的混合溶液,辅助结合溶剂的体积为裂解液体积的0.6-0.8倍;所述3D打印特形 功能体进行核酸的结合,结合时间为5s-5min。 上文所述的技术方案中,步骤(3)所述进行核酸的清洗,具体为,将结合有目标核 酸的3D打印的特形功能体的手柄区端通过人工或机械移动至预置有清洗液的容器中,使核 酸结合区伸入清洗液中进行核酸的清洗,使3D打印特形功能体在清洗液中进行搅动。所述 步骤(3)中的清洗一般为1-5次;所述清洗时间为每次2s-1min;优选的,所述清洗液包括70- 80%的酒精。 上文所述的技术方案中,步骤(4)所述的干燥过程可在室温或加热下进行,干燥过 程时间为1min-2h; 上文所述的技术方案中,步骤(5)所述洗脱,洗脱时间为5s-5min,洗脱液可以是适 宜浓度或者便于储存的高浓度的水、PBS、TE缓冲液和下游PCR反应液等,优选的,本发明采 用TE缓冲液,TE缓冲液的具体组分为:10mMTris-HCl,1mM EDTA(PH=8.0)。 本发明还提供了基于3D打印特形功能体的血液基因组DNA提取方法的应用试剂 盒。具体的,试剂盒中包含如下组分: (1)3D打印特形功能体; (2)裂解液 (3)蛋白酶K; (4)RNA消化酶 (5)清洗液; (6)洗脱液; (7)固定架; (8)操作说明书。 所述3D打印特形功能体为以光敏树脂或热塑性塑料为原料,通过3D打印技术获得 的由核酸结合区和手柄区组成的、具有“伞”型结构的微元件,并通过连接区将若干“伞”型 结构的微元件并排连接;所述裂解液包括CTAB裂解液、NaHCO3裂解液、Chelex裂解液、蛋白 酶K裂解液或SDS裂解液中的一种;所述清洗液包括70-80%的酒精;所述洗脱液包括水、 PBS、TE缓冲液和下游PCR反应液中的一种;所述固定架为可以固定、排布若干个3D打印特形 功能体的结构。 所述3D打印特形功能体为如前文所述的任意一种结构,优选的为如图1(b)所示的 匹配8联排管使用的含有8个核酸结合区的结构,需要单个使用时,可以掰下来使用;所述固 定架为可以固定、排布数个3D打印特形功能体的结构,使得多个3D打印特形功能体可以随 着固定架同时移动,匹配多孔板或者多个离心管使用。 有益效果:本发明所提供的获取血液DNA的方法,能够高效、简便、快速、高通量的 提取、分离目标DNA,具有明显先进于现行技术的优势: 6 CN 111607635 A 说 明 书 4/7 页 1)本发明所提供的血液DNA提取方法,采用3D打印特形功能体进行核酸的分离与 纯化,通过机械力快速转移3D打印特形功能体完成,避免了传统非磁力核酸固相分离依赖 多步离心与移液操作的瓶颈制约,显著节约劳动力;同时,3D打印特形功能体可以匹配8联 排管、96孔板或者384孔板使用时,实现高通量操作,这是对现行提取技术普遍通量低的一 个重要突破; 2)本发明所提供的血液DNA提取方法,采用3D打印特形功能体进行核酸的分离与 纯化,是一种固相核酸分离方法。固相核酸分离中,磁力分离被普遍认为快速且具有高通 量,而本发明所述方法可以获得比磁力分离更快的分离速度、更简单的操作过程和更稳定 的分离效果。利用3D打印特形功能体进行核酸的分离,1-5min内可以从裂解液中分离、纯化 出核酸,且不需要移液、离心等繁琐耗时的操作;而采用磁力分离通常需要14.5min左右,且 需要多次移液操作(Zou Y,Mason MG,Wang Y,Wee E,Turni C,Blackall PJ,et al.(2017) Nucleic acid purification from plants ,animals and microbes in under 30 seconds.PLoS Biol 15(11):e2003916.)。同时,采用3D打印完全不存在因磁珠颗粒沉降、 聚集等问题引起的核酸结合不充分和杂质包裹等问题,有效保障了核酸提取的稳定性和质 量; 3)本发明所提供的3D打印特形功能体的原材料便宜、易得;打印过程方便、快速, 能显著降低了经济成本; 4)本发明所提供的血液DNA提取方法,不依赖离心、移液等繁琐操作,可以实现人 工低劳动密度高通量核酸分离,且整个过程能够在1m2的操作环境下完成,节约空间,使用 灵活性高;同时,基于3D打印特形功能体的血液提取方法又可以通过设计程序化的设备进 行3D打印特形功能体在裂解液、清洗液及洗脱液之间的转移,实现自动化,进一步降低人力 成本,将有利于推动下游分子技术,尤其血液中致病性病原的精准、快速诊断,如疟原虫PCR 体外诊断的临床应用。 附图说明 图1是本发明3D打印特形功能体的结构示意图,(a)为单体3D打印特形功能体,(b) 为八联3D打印特形功能体。 图2是本发明实施例2的琼脂糖凝胶电泳图,图中泳道1-4为恶性疟3D7株滤纸血1 ~4号样本,泳道5-8为感染间日疟原虫病人滤纸血5~8号样本,泳道M为DL2000 Marker。 图3是本发明实施例3的琼脂糖凝胶电泳图,图中泳道1-8为感染杆状病毒柞蚕蛹 血液1~8号样本,泳道M为DL2000 Marker。 图中,1、核酸结合区;2、手柄区;3、连接区。












